Содержание
Прослеживается известная преемственность между концепцией интестинальной интоксикации и гипотезой о связи между микрофлорой толстого кишечника и канцерогенезом. Она основана на наблюдениях о том, что бактерии толстого кишечника способны трансформировать эндогенные соединения и вещества, поступающие с пищей, в канцерогенные или коканцерогенные факторы, которые действуют на кишечник или, проникая в кровь, вызывают злокачественную трансформацию клеток других тканей. Примером является канцерогенная трансформация пищевых добавок типа цикломатов, стероидных гормонов, желчных кислот и др. Так, цикломат (циклогексамин сульфат) под влиянием бактериальных сульфатаз превращается в циклогексамин — сильный канцероген для эпителиоцитов мочевого пузыря. Значение подобных конверсий не известно, но они привлекают внимание современных онкологов.
Пожалуй, наиболее реальным является участие нормальной микрофлоры в развитии оппортунистических инфекций. Еще Ш. Николь говорил о «микробах выхода» (microbes de sortie), имея в виду условную патогенность большинства представителей эндогенной микрофлоры, которые способны активно или пассивно покидать место своей обычной дислокации, проникая в стерильные участки тела или внедряясь в чужие микробиоценозы. Это наблюдается в разных ситуациях: при перфорации стенки кишечника, повреждении кожи и слизистых оболочек, при восходящей инфекции мочевыводящей системы и пр. Вирулентность бактерий в сочетании с ослаблением местной и общей резистентности организма способствуют закреплению «микробов выхода» и реализации их патогенетического потенциала. Мы говорили об этом ранее с позиций общепринятой концепции оппортунистических инфекций. Некоторые из наиболее последовательных апологетов дисбактериоза относят к нему чуть ли не все оппортунистические инфекции.
При этом предполагается, что выходящие из-под контроля условно-патогенные бактерии гиперрепродуцируются не только в зоне своего естественного обитания, но и проникают в другие органы, инициируя инфекционный процесс. Вряд ли, однако, можно согласиться с тем, что, например, септическая инфекция мочевыводящих путей, вызванная кишечной палочкой, является результатом декомпенсированного дисбактериоза кишечника. Пиогенные бактерии, не дожидаясь дисбактериоза, постоянно проникают в систему мочевыделения из перианальной зоны, но быстро удаляются из мочевыводящего тракта, не успев спровоцировать воспалительную реакцию. Условия для их патогенетически значимого размножения возникают лишь при механической задержке мочи, травмировании слизистой оболочки диагностическими или лечебными процедурами, повышенном содержании в моче глюкозы (отличного продукта питания для бактерий). То же самое справедливо и для других «внекишечных проявлений дисбактериоза». Вряд ли, например, разумно лечить пиелонефрит или септическую инфекцию легких препаратами, нацеленными на восстановление микрофлоры кишечника. Если она и нарушена, то это вторичное явление, исчезающее вместе с ликвидацией базисного патологического процесса. Кстати, нечто подобное справедливо и для дисбактериоза самого кишечника. Некоторые авторы дифференцируют дисбактериозы кишечника по этиологическому принципу — протейный, клебсиеллезный, стафилококковый, бактероидный, синегнойный и пр. Но если этиологическая значимость соответствующих бактерий в кишечных расстройствах больного доказана (что сделать довольно трудно), проще говорить об инфекции, а не о дисбактериозе и лечить пациента, исходя из общих принципов антибактериальной терапии.
Формально любую экзогенную инфекцию можно рассматривать как дисбактериоз или дисбиоз, так как всякое экзогенное заражение сопровождается появлением в организме количественно и/или качественно новых микробиоценозов, т.е. изменением микрофлоры. Безусловно, дисбактериоз как один из механизмов нарушения колонизационной резистентности может стать основой для оппортунистических инфекций кишечника (как это установлено для C. difficile), но внекишечная локализация «кишечных бактерий» не обязательно является фазой местного дисбиотического процесса. Скорее наоборот: перекосы в микрофлоре, регистрируемые в таких случаях, возникают как вторичная реакция на изменения экологии кишечника, спровоцированные дистантным инфекционным процессом. Иными словами, являясь реальной микробиологической категорией, кишечный дисбактериоз несет в подобных ситуациях сомнительную патогенетическую нагрузку.
Дисбактериоз как индикатор здоровья
В наиболее общем виде можно говорить о двух механизмах нарушения нормальной микрофлоры. Один из них связан с выбиванием бактерий антимикробными препаратами, прежде всего антибиотиками. Второй является следствием реактивной перестройки микрофлоры в ответ на изменения той среды, где сосредоточен данный микробиоценоз. Как уже отмечалось, сдвиги в микрофлоре кишечника наблюдаются при многих заболеваниях, в том числе внекишечной локализации. Это означает, что кишечник меняет свою экологию, реагируя на разнообразные нарушения гомеостаза. Отсюда дисбиотические реакции следует считать косвенным отражением такого рода дестабилизационных процессов. Они не ограничиваются перекосами в микрофлоре кишечника, но проявляются и в других участках тела. Это объясняется тем, что изменение состояния организма в той или иной мере сказывается на всех отделах слизистой оболочки и кожи, обеспечивая синхронность дисбиотических реакций разной локализации, а также пассивных сдвигов в микрофлоре, возникающих на фоне антибактериальной терапии. Парадокс, но заключение о норме или патологии микробиоценоза толстого кишечника с известной долей вероятности можно сделать по результатам анализа микрофлоры ротоглотки, буккального эпителия и даже кожи.
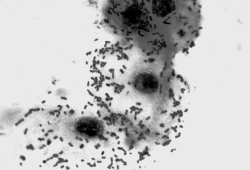
В целом, перестройку в нормальной микрофлоре можно использовать как критерий для суждения о состоянии здоровья, его явных и скрытых нарушениях, о позитивных и негативных тенденциях в развитии патологического процесса и адекватности проводимой терапии. Громоздкость бактериологического анализа фекальной микрофлоры практически исключает такую возможность, тем более что наблюдение необходимо вести в динамике. В связи с этим представляет интерес тестирование микробиоценозов других участков тела. В свое время широко практиковалось изучение микрофлоры кожи при помощи удобного технического приема, предложенного Н.Н. Клемпарской. Нами используется тест на естественную колонизацию буккального эпителия, который в норме обильно заселен оральными стрептококками. Снижение этого показателя и обсеменение буккальных эпителиоцитов посторонней микрофлорой наблюдается при различных заболеваниях, сигнализируя о дестабилизации гомеостаза на уровне слизистых оболочек (см. рисунок).
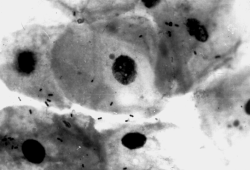
Естественная колонизация буккального эпителия: а — здоровый донор (12 лет), эпителиоциты обильно колонизированы оральными стрептококками; б — ребенок (4 года) с бронхиальной астмой, резкое снижение количества оральных стрептококков. х630 (препараты М.А. Абаджиди)
Дисбактериоз как объект терапии
Один из принципов утилитарной врачебной логики состоит в том, что все показатели, отличающиеся от условной нормы, требуют коррекции. При этом не учитывается вторичность многих сдвигов, имеющих скорее адаптивный, чем патогенетический характер. Ликвидация базисного процесса автоматически устраняет такого рода псевдонарушения. По сути это символы патологии, а не патогенетические детерминанты, требующие врачевания. Именно с таких позиций следует подходить к целесообразности направленной коррекции дисбиотических состояний, которые сопутствуют многим нарушениям гомеостаза.
Необходимы критерии, по которым можно было бы судить о том, когда дисбиозы переходят грань адаптивной реакции и трансформируются в патогенетически значимый механизм. Собственно на это нацелены все классификации кишечного дисбактериоза, подчеркивающие опасность глубоких перестроек резидентной флоры. Наиболее логичной выглядит заместительная терапия живыми бактериями, населяющими толстый кишечник. Препараты, изготовленные на их основе, получили название пробиотиков, или эубиотиков, так как они нацелены на восстановление эубиотического (нормального) состояния микрофлоры. В коммерческом варианте такие препараты доступны в виде колибактерина (живая кишечная палочка), бифидумбактерина (бифидобактерии), лактобактерина (лактобациллы) и их комбинаций (бификол, бифилакт); в последнее время стал рекламироваться препарат на основе энтерококка. Все они применяются в форме лиофилизированных живых бактерий либо в виде продуктов, приготовленных путем сбраживания молока соответствующими бактериями. Много усилий потрачено на поиски оптимальных штаммов, обладающих антагонистическими (по отношению к потенциально опасным бактериям) свойствами, устойчивостью к антибиотикам, активно сбраживающих молоко и пр. Общая идея сводится к искусственному заселению кишечника «благородными» бактериями, вытеснению благодаря этому болезнетворных штаммов и восстановлению нормального микробиоценоза (эубиоза). Огромный опыт, зафиксированный в необозримом количестве публикаций, свидетельствует о положительном эффекте бактериотерапии при хронических заболеваниях кишечника и их системных осложнениях (например, при аллергодерматозах). С такой же целью и с неменьшим успехом предложено использовать добавки к питанию (пробиотики), стимулирующие размножение полезных бактерий, прежде всего бифидобактерий (бифидогенные факторы или бифидогенный режим).