Содержание
Вирус гепатита В — один из мельчайших оболочечных вирусов человека. Его вирион (частица Дейна) имеет сферическую форму диаметром 40—45 нм. Под электронным микроскопом в вирионах отчетливо видны сердцевина (кор, т.е. нуклеокапсид) и наружная липопротеиновая оболочка (суперкапсид) (рис. 2).
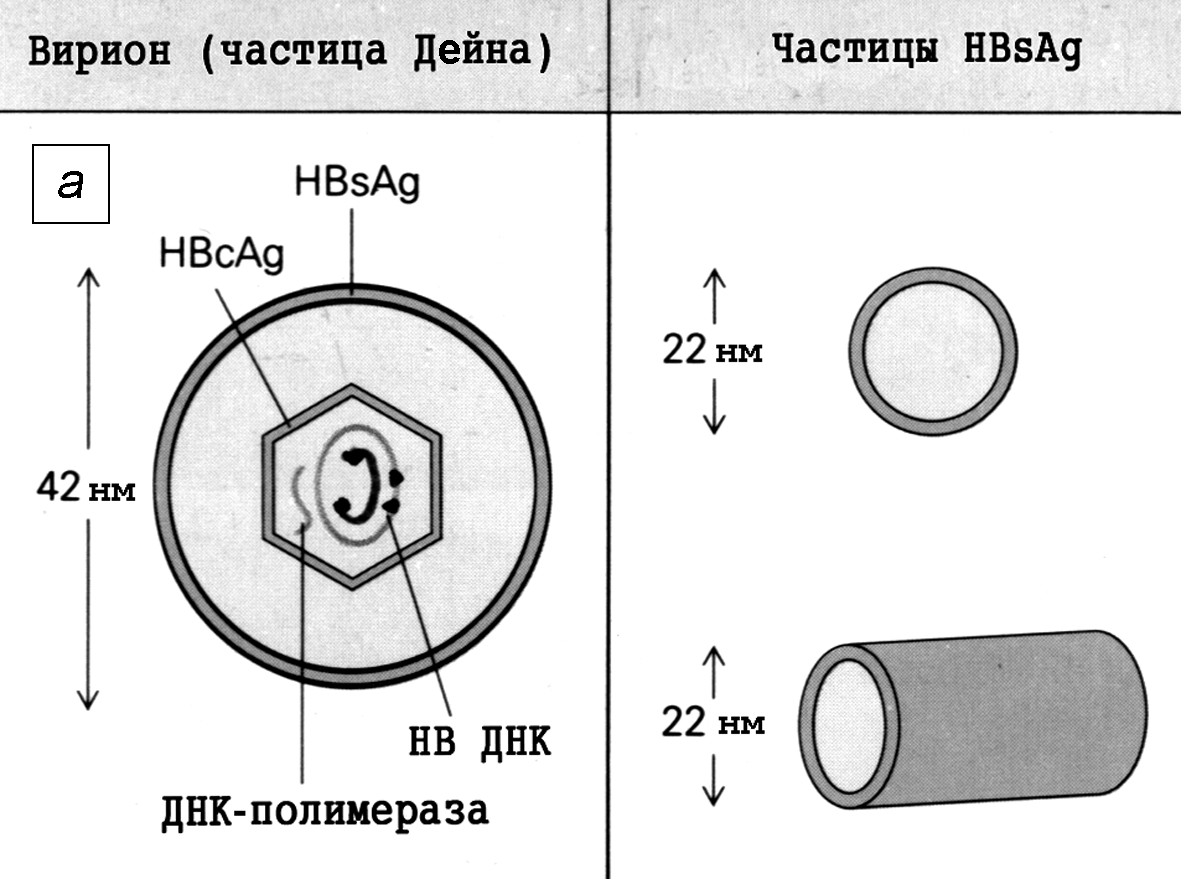
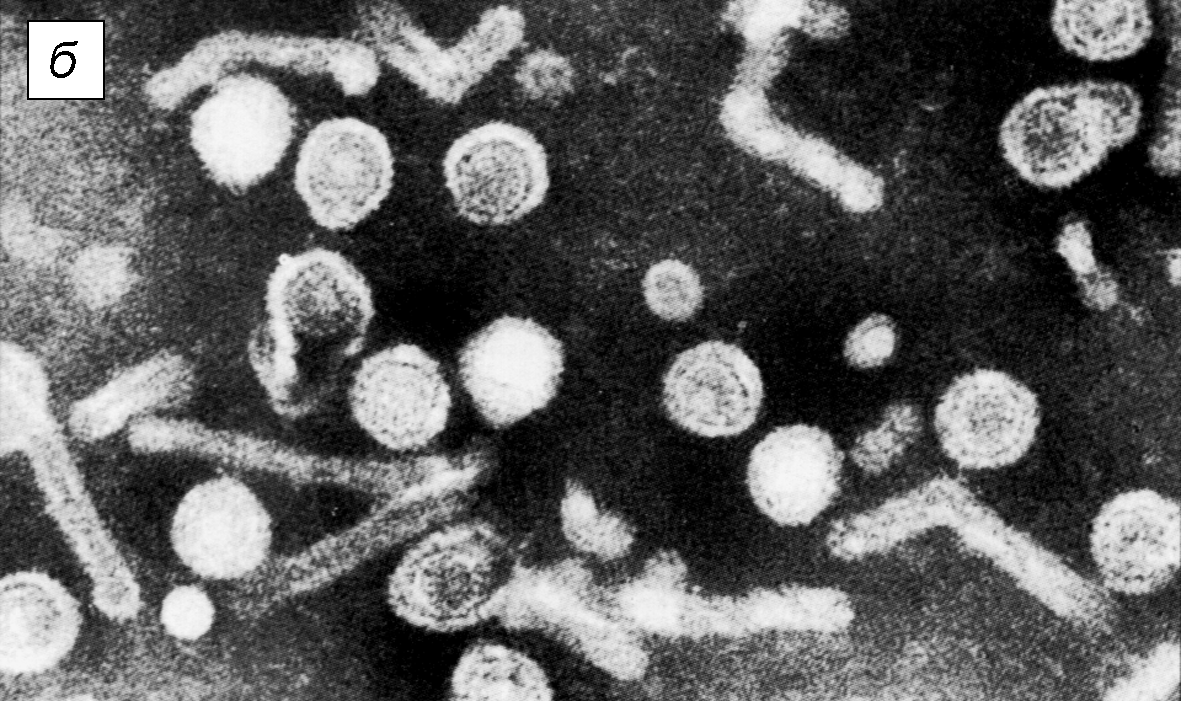
Рис. 2. Вирион вируса гепатита В (частица Дейна) и HВsAg-частицы:
а — принцип строения; б — электронограмма крови больного
Вирусные белки. Вирус обладает пятью белковыми антигенами: HBsAg, HbcAg, HBeAg, HBxAg и HBpol.
HBsAg (устар. австралийский антиген) — поверхностный антиген (s от англ. surface — поверхность). Обеспечивает избирательное прикрепление вируса к мембране гепатоцитов, возможно за счет связывания с полимеризованным сывороточным альбумином.
Понятие «HBsAg» объединяет три оболочечных гликозилированных белка — S, M и L. Они являются производными s-гена и прилежащих к нему коротких ДНК-фрагментов, pre-s1 и pre-s2. Их экспрессия дает три продукта — HBsAg-S (производное s-гена; англ. short — короткий), HВsAg-M (продукт s- и pre-s1; англ. middle — средний) и НВsAg-L (продукт s-, pre-s1 и pre-s2; англ. long — длинный, большой). В вирионе 70% приходится на HВsAg-S — главный оболочечный антиген. НВsAg-M и HBsAg-L cоставляют примерно 30% поверхностного белка. HBsAg-L принимает участие в стыковке суперкапсида с кором и, возможно, в рецепции вириона клетками печени. Функции HBsAg-M не известны.
HBsAg cодержит протективные В-эпитопы и индуцирует синтез антител, блокирующих прикрепление вируса к рецепторам гепатоцитов. Синтезируется в избытке (особенно при интегративной инфекции — см. ниже) и в значительных количествах секретируется в кровь, где определяется не только в структуре вирионов, но и в виде свободных агрегатов (сферические частицы, филаменты), состоящих из S- и L-белков. Их количество во много раз превосходит число полноценных вирионов, достигая 1012 в 1 мкл сыворотки (см. рис. 2).
По HВsAg-эпитопным особенностям дифференцируют четыре основных HBV-серовара, которые используются как эпидмаркеры. По меньшей мере один из эпитопов (a) является общим для всех штаммов вируса, что обеспечивает возможность универсальной диагностики, основанной на выявлении HВsAg в сыворотке, а также применение стандартной HВsAg-вакцины для профилактики гепатита В.
HВcAg, или кор-антиген — главный белок HBV-нуклеокапсида, или сердцевины (англ. core — сердцевина). Кодируется c-геном, к которому прилежит небольшой, но функционально значимый фрагмент ДНК — пре-c. От того, с какого участка пре-c начинается транскрипция мРНК, зависит качество и судьба НВсAg. Один из его вариантов входит в состав вирионного нуклеокапсида, другой (гидрофобный) включается в клеточные мембраны и служит объектом для распознания и атаки Т-лимфоцитами. В кровь не секретируется и в свободном состоянии не определяется.
HBeAg — важный для диагностики (и, по-видимому, для репликации вируса) продукт c-гена (англ. envelope — оболочка). Образуется в результате протеолиза (возможно, аутопротеолиза) кор-антигена, встроенного в клеточные мембраны. Отличается от последнего по В-эпитопам (т.е. к каждому из них образуются собственные антитела), но содержит общие с ним Т-эпитопы. Не входит в состав вириона, а выделяется в кровь, где его содержание коррелирует с активностью вирусной репликации.
HBхAg — неструктурный белок. Определяется в сыворотке и печени при высоком уровне вирусной репликации. Выполняет функции трансактиватора вирусных и клеточных генов, способствуя развитию патологического процесса в печени. Его производные определяются в мембране гепатоцитов почти у половины больных хроническим гепатитом, являясь объектом для цитотоксических Т-лимфоцитов. Полагают, что наряду с инсерционным мутагенезом (результат внедрения/инсерции вирусного генома в хромосомы клетки) HBxAg участвует в индукции злокачественного перерождения HBV-инфицированных гепатоцитов, активируя клеточные онкогены и блокируя антионкогенные (апоптозиндуцирующие) белки, в частности р53.
HBVpol (полимераза) — полифункциональный фермент, входящий в состав HBV-сердцевины. Продукт самого крупного, р-гена, перекрывающего s- и c-локусы. Обладает активностью ДНК-полимеразы, обратной транскриптазы и РНК-азы (см. ниже). Играет ключевую роль на всех этапах репликации вируса.
Геном. Геном гепаднавирусов устроен своеобразно. Он состоит из двух ковалентно незамкнутых нитей ДНК, одна из которых (плюс-нить) не достроена, т.е. короче другой (минус-нити) на 20—30%. Ликвидация этого дефекта является обязательным этапом репликации вируса и обеспечивается вирионной ДНК-полимеразой после проникновения вируса в ядро гепатоцитов. Каждому из главных вирусных белков соответствует открытая рамка считывания (фактически ген), но небольшой размер генома (3,2 кбайт, т.е. меньше, чем у любого из известных вирусов с двухспиральной ДНК) не позволяет синтезировать даже столь скромный набор антигенов без дополнительных ухищрений, нацеленных на увеличение генетической емкости ДНК. Это достигается путем транскрипции с перекрывающихся областей ДНК (перехлест генов) и сдвига рамок трансляции мРНК-транскриптов. Кроме того, синтезированные полипептиды подвергаются посттрансляционным модификациям (ограниченному протеолизу, гликозилированию), меняющим их структуру и функции.
Репликативная инфекция. Репликация HBV происходит необычно. Это единственный из ДНК-вирусов человека, который реплицируется с подключением механизма обратной транскрипции по схеме ДНК—РНК—ДНК (рис. 3). После достраивания в ядре дефектной ДНК-нити она используется клеточной РНК-полимеразой в качестве матрицы для синтеза полной РНК-копии — прегенома (pgRNA). Одновременно образуются и более короткие РНК, которые подвергаются трансляции, обеспечивая синтез вирусных белков. pgRNA транспортируется в цитоплазму и после объединения с капсидом переписывается в ДНК, т.е. подвергается обратной транскрипции. РНК разрушается, и на свободных участках ДНК строится вторая (дефектная) ДНК-нить.
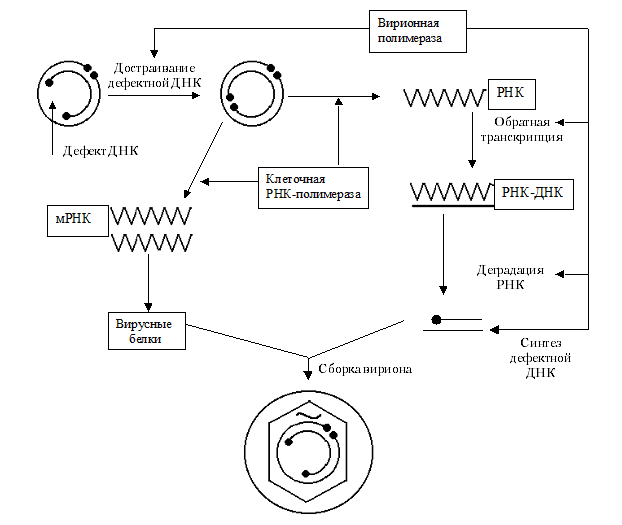
Все перечисленные этапы (достраивание дефектной ДНК-нити, обратная транскрипция, разрушение pgRNA, синтез дефектной ДНК-нити) обеспечиваются общим ферментом — вирионной полимеразой. Полифункциональность снижает точность ферментативных реакций. Весомость ошибок возрастает, если они (как в данном случае) допускаются при репликации. С этим, в частности, может быть связана высокая мутационная изменчивость HBV, которая накладывает серьезный отпечаток на взаимоотношения с хозяином. Механизм обратной транскрипции сближает гепаднавирусы с ретровирусами. По этой причине их даже предложено называть параретровирусами.
Процесс репликации заканчивается сборкой суперкапсида. Кор одевается наружной оболочкой, используя для этого внутриклеточные мембраны аппарата Гольджи с встроенными в них HВsAg (S, L и М), и высвобождается из клетки.
Интегративная инфекция. Кроме репликативной инфекции, которая ведет к воспроизведению вирионов, вирус гепатита В имеет в арсенале еще одну стратегию — он охотно встраивает свою ДНК в геном зараженной клетки, используя ее как прикрытие. Этот механизм, хорошо известный в вирусологии, носит название интегративной вирогении. Не обеспечивая репродукции (хотя такая возможность остается), он способствует длительному сохранению (персистенции) вируса в инфицированных клетках, что поддерживает его патогенетический потенциал. Экспрессия вирусных генов блокируется; исключение составляют s- и, по-видимому, x-гены. Транскрипция s-гена даже усиливается, если он попадает под контроль клеточных генов-промоторов. Образующийся в избытке HBsAg не накапливается в гепатоцитах, а в больших количествах выделяется в кровь. При хроническом гепатите репликативная и интегративная инфекции развиваются параллельно, но со временем верх берет интегративный компонент, который существенно влияет на развитие цирроза печени и первичной гепатомы.