Содержание
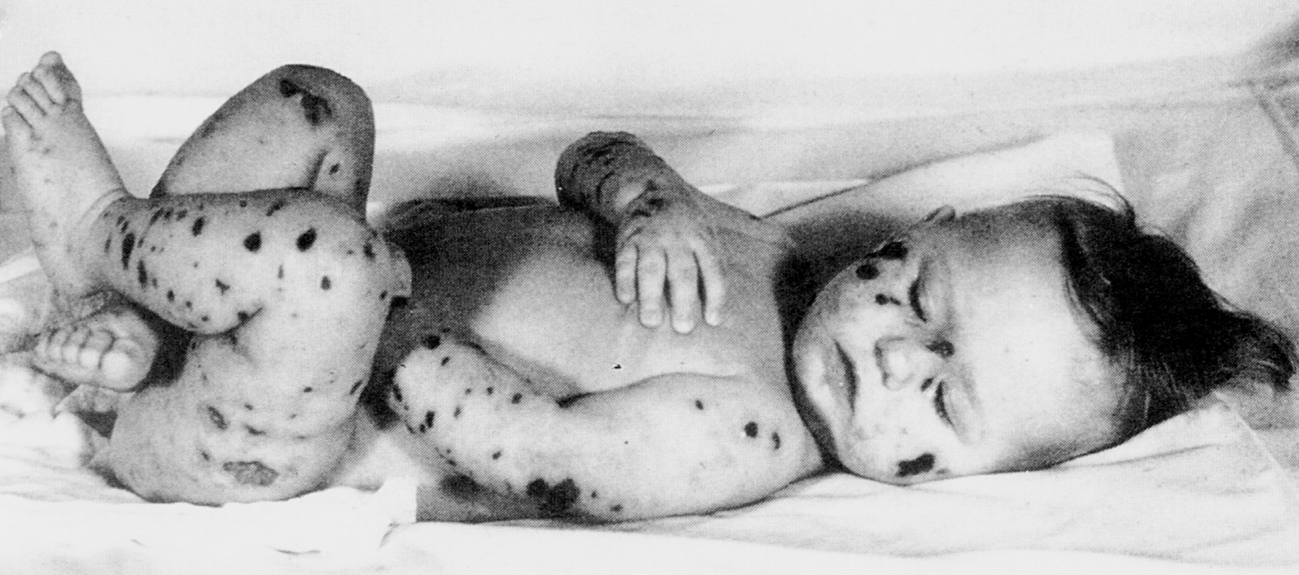
Но главное в том, что, преодолев бактерицидность крови, менингококк размножается и, накапливаясь в огромных количествах, высвобождает большую массу эндотоксина в виде мембранных пузырьков. Этому способствуют склонность менингококка к аутолизу и комплементзависимый бактериолиз. Гиперэндотоксинемия ведет к острейшему синдрому внутрисосудистой активации крови, характерному для септических состояний (см. «Сепсис»). Обычным спутником менингококцемии является геморрагическая сыпь (рис. 4), реже возникают молниеносный коллапс и смерть из-за тромботического некроза надпочечников (синдром Уотерхауза—Фридрихсена). В пораженных участках (например, в очагах кожной сыпи) обнаруживаются менингококки, которые благодаря кровоизлияниям из тромбированных сосудов получают доступ в ткани.
Поражение мозга по сути отражает сходный тромбогеморрагический процесс в сосудах мозговых оболочек. В цереброспинальной жидкости бактерии находят отличные условия для размножения. Здесь достаточное количество питательных веществ, но практически нет опсонинов (комплемента, антител) и фагоцитов. Это обеспечивает беспрепятственное размножение бактерий, которое на 12 ч и более опережает массированный выход нейтрофилов из циркуляции. Благодаря воспалительной реакции цереброспинальная жидкость обогащается белками плазмы, в том числе опсонинами. Бактерии подвергаются опсонофагоцитарной атаке, которая, запаздывая, не всегда обеспечивает выздоровление.
Попытки найти специализированные факторы, способствующие закреплению менингококков на мозговых оболочках, не увенчались успехом. Известно лишь о перестройке цитоскелетного аппарата эндотелиальных клеток и их возможных, в том числе бактериальных, механизмах. Дело, по-видимому, ограничивается контактной болезнетворностью для эндотелиоцитов (хотя геном N. meningitidis не содержит генов, кодирующих систему секреции типа III) и трансцитозом, прежде всего в зоне хориоидного сплетения. Инвазию, как в случае с эпителием, скорее всего начинают бактериальные пили и CD46 эндотелиоцитов. После редукции пилей к реакции подключаются белки наружной мембраны и, возможно, другие факторы, в частности бактериальная IgA-протеаза, содействующая внутриклеточному выживанию менингококка. Впрочем, подобные поиски, возможно, излишни, так как инфицированные тромбы, образующиеся в сосудах, сами по себе — отличный субстрат для бактериальной колонизации.
Выявление грамотрицательных диплококков при микроскопии мазка из спинномозговой жидкости служит стопроцентным подтверждением диагноза менингококкового менингита (рис. 5).
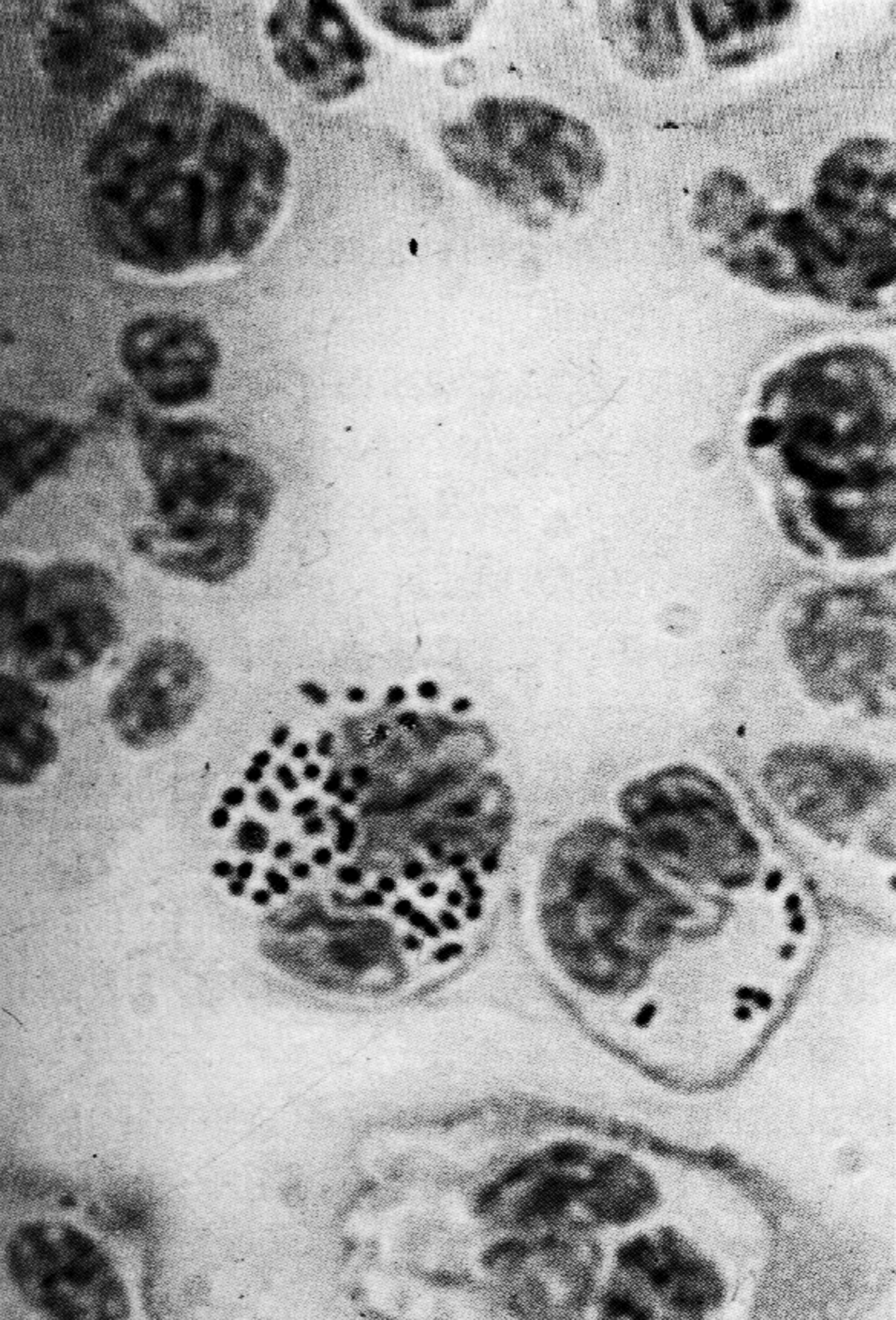
Бактерии лежат свободно или находятся внутри нейтрофилов. Помогает выявление менингококковых антигенов в реакции агглютинации микрочастиц, нагруженных антименингококковыми антителами. Менингококк может быть выделен из крови, спинномозговой жидкости, кожных экзантем, носоглотки. В последнем случае его приходится дифференцировать от непатогенных нейссерий, постоянно обитающих в верхних дыхательных путях.
Утверждение представлений о протективности противокапсульных антител явилось основой для разработки вакцин из очищенных капсульных полисахаридов наиболее распространенных серогрупп менингококка (А, В, С). Однако их внедрение столкнулось с рядом трудностей. Полисахарид В, являясь полимером сиаловой кислоты, оказался слабым иммуногеном для человека, а полисахарид С лишен протективного эффекта у детей до двух лет (возможно, по причине Т-независимости), хотя именно в этом возрасте около 30% заболеваний связано с данной разновидностью менингококка. Предложены химические модификации В-полисахарида и его конъюгаты с белковыми носителями, стимулирующие синтез протективных антител, но, в целом, высокоэффективная вакцинация остается делом будущего. Есть предложение использовать с этой целью поверхностные трансферинсвязывающие белки, которые индуцируются во время инфекции. Антитела к трансфериновым рецепторам (прежде всего к Tbp2) блокируют связывание трансферина, обладая бактерицидностью. Принципиально, что по антигенной специфичности трансферинсвязывающие белки одинаковы у большинства штаммов менингококка. В перспективе это определяет широкий спектр вакцинального эффекта. Впрочем, учитывая невысокую заболеваемость и ее редкие подъемы, введение плановых прививок вряд ли целесообразно. Их следует проводить скорее по эпидемическим показаниям, т.е. в период вспышек. Полезно помнить и о том, что сывороточные антитела, защищающие от внутрисосудистой инвазии, не предохраняют от носительства менингококка, а потому не способны обеспечить искоренения инфекции.
Во многих случаях спасает то, что менингококки сохраняют чувствительность к пенициллину, современные разновидности которого, наряду с новыми поколениями цефалоспоринов, остаются лучшим средством этиотропной терапии. Хотя и с большими потерями, антибиотики проходят через гематоэнцефалический барьер, достигая бактерицидных концентраций в цереброспинальной жидкости. Этому способствует повышение проницаемости сосудистых сплетений головного мозга на фоне воспаления — именно через них идет формирование основной массы тканевой жидкости и вместе с ней поступление в ЦНС лекарственных препаратов. Массовый бактериолиз, индуцируемый антибиотиками, может спровоцировать высвобождение больших количеств эндотоксина. Этим объясняется временное ухудшение состояния некоторых больных после первых инъекций антибиотиков. Поэтому в целях безопасности их применяют одновременно с кортикостероидными гормонами, которые сглаживают действие флогогенных цитокинов, опосредующих септические эффекты эндотоксина.
Гонококк
Мала причина, да грех велик.
- Особенности микробиологии.
- Эпидемиология мужской и женской гонореи.
- Адгезины и колонизация эпителия.
- Инвазивность и пиогенность.
- Острая гонорея и патогенез осложнений.
- Механизмы персистенции и хронической гонореи.
- Проблемы лечения и профилактики.
Г онорея — одна из самых распространенных инфекций человека, передаваемых половым путем. В переводе с греческого гонорея означает истечение семени. Название болезни, предложенное Галеном за 130 лет до н.э., с патогенетической точки зрения ошибочно (истекает не семенная жидкость, а гной), но отлично отражает один из главных симптомов острой инфекции у мужчин — обильное выделение гнойного экссудата из мочеиспускательного канала при остром гонорейном уретрите. Еще образнее немецкое наименование болезни — триппер (от нем. trippen — капать). Оба термина символизируют мужскую гонорею; у женщин заболевание протекает менее остро, нередко в скрытой форме. Впрочем, это не делает женскую гонорею менее опасной. Инфекция обретает коварный характер, создавая опасность осложнений и затрудняя контроль за распространением.
Острая гонорея может переходить в хроническую форму, которую непросто диагностировать и трудно лечить. Вялотекущее гнойное воспаление распространяется на различные отделы полового тракта, соседние ткани и имеет тяжелые последствия, связанные с реактивным разрастанием фиброзной ткани — склерозом. Изредка гонорея осложняется септикопиемией с преимущественным поражением суставов, клапанов сердца, аорты, кожи. Яркой манифестацией экстрагенитальной гонореи является гнойный конъюнктивит, или бленорея (от греч. blennos — слизь и rheo — теку). Кроме взрослых, бленореей болеют новорожденные, заражаясь в родовом канале матерей, инфицированных гонококком.
Возбудитель открыт в 1879 г. А. Нейссером. Он сообщил о диплококках, в большинстве располагающихся внутриклеточно, обнаруженных им у всех больных с острым уретритом и бленорейным воспалением глаз (рис. 1). А. Нейссер предложил называть вновь открытые бактерии гонококком или гонорейным диплококком. Вскоре были получены чистые культуры гонококка и при заражении ими добровольцев воспроизведена гонорея (гонорейный уретрит). Это окончательно утвердило за диплококком Нейссера роль возбудителя гонореи. Гонококк является строгим паразитом человека, хотя в эксперименте гонорею удается вызвать у приматов, в частности шимпанзе. Они не только «болеют» гонореей, но и передают ее половым партнерам.