Содержание
О присутствии H. pylori в желудке (12-перстной кишке) судят по следующим критериям: 1) получение культуры из эндоскопических биоптатов; 2) микроскопия отпечатков биоптатов слизистой оболочки; 3) определение уреазной активности в биопсийном материале или содержимом желудка; 4) выявление антител к хеликобактерным антигенам; 5) тестирование исследуемого материала на присутствие хеликобактерной ДНК.
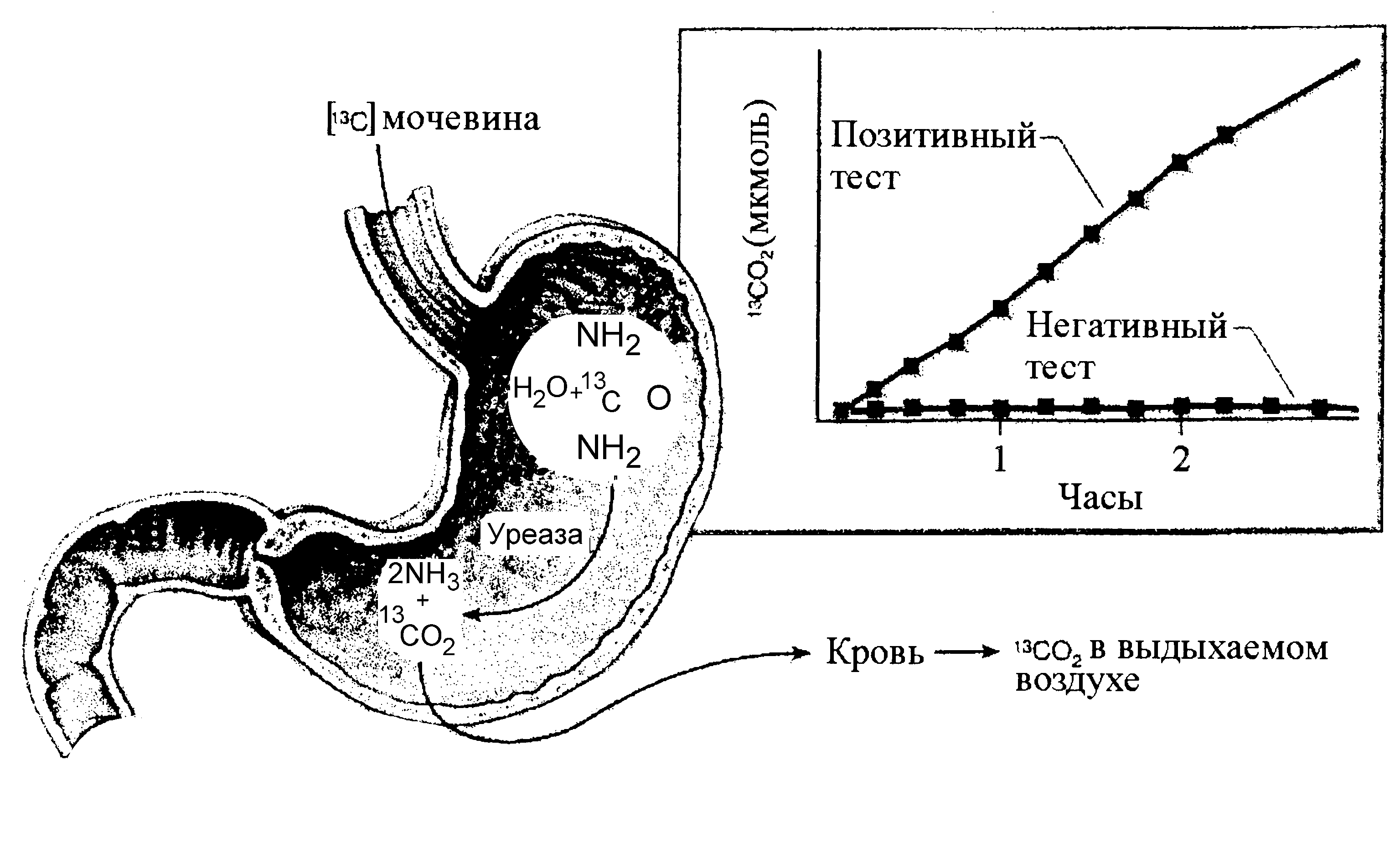
Один из главных недостатков эндоскопического исследования — инвазивность. Кроме того, при эндоскопии можно не угадать место для взятия биоптата и получить ложноотрицательный результат. Этих недостатков лишен остроумный способ диагностики хеликобактерной инфекции — респираторный тест с мочевиной. Он основан на неинвазивном выявлении уреазной активности в желудке, единственным источником которой является H. pylori. Обследуемый принимает с пищей мочевину, меченную радиоактивным углеродом. Под влиянием уреазы она разлагается на аммиак и углекислый газ, который всасывается в кровь, выделяясь легкими. Его регистрируют в выдыхаемом воздухе, начиная с первых минут после приема мочевины (рис. 3). Метод высоконадежен, так как отражает суммарную метаболическую активность бактерий, независимо от места колонизации в желудке.
У лиц, инфицированных H. pylori, образуются антитела против различных антигенов H. pylori. Их можно обнаружить в крови и слюне. на этом основана иммунодиагностика хеликобактерной инфекции. Определение сывороточных антител при помощи иммуноферментного анализа по специфичности и чувствительности почти не уступает эндоскопическому обследованию и дыхательной пробе с мочевиной. Такие тесты дешевле и достаточно надежны для выявления инфекции у нелеченых больных. К недостаткам метода относится инерционность: результат остается положительным не менее месяца после ликвидации инфекции. Это затрудняет слежение за эффективностью антибактериальной терапии и полнотой элиминации возбудителя.
Вызывает интерес диагностика хеликобактерной инфекции при помощи полимеразной цепной реакции, которая с предельной чувствительностью позволяет судить о присутствии H. pylori по фрагментам его генома в желудочном соке (в частности генов уреазы — ureA, ureB, ureC).
Открытие хеликобактерной инфекции радикально изменило подходы к лечению больных с язвенной болезнью желудка и 12-перстной кишки: традиционная патогенетическая (антисекреторная) терапия сегодня неизменно сочетается с применением этиотропных (антибактериальных) средств. H. pylori быстро теряет чувствительность к антибиотикам, если они применяются раздельно. В связи с этим предложены разнообразные комбинации и схемы применения антибиотиков и других антибактериальных препаратов, которые во многих случаях позволяют элиминировать H. pylori из организма, создавая условия для выздоровления. Основным требованием является полное искоренение инфекции, о чем в идеале можно судить по негативным результатам микробиологического анализа на протяжении как минимум четырех недель после завершения курса лечения. Впрочем, обычно полагаются на отсутствие рецидивов, и только при их появлении обследование повторяют. Сегодня антибактериальная терапия занимает 1—2 нед, что является большим достижением по сравнению с несколькими месяцами лечения, которое применялось ранее.
Известные надежды связаны с вакцинацией, хотя длительное выживание H. pylori на фоне естественного иммунного ответа заставляет сомневаться в реальности подобной перспективы.
Хеликобактерная инфекция — один из самых популярных объектов современной бактериологии. Интрига сюжета, его актуальность, вызов классическим традициям, противоречия, оставляющие надежды скептикам — все это побуждает к новым изысканиям, которые непрерывно расширяют концептуальные контуры, впервые заложенные чуть более двадцати лет назад. Многое подлежит уточнению, возможны очередные компромиссы. Серьезных последствий, например, следует ожидать от изучения внутривидовой неоднородности H. pylori конституционального и индуцибельного (адаптивного) характера. Это поможет разрешить главное противоречие — бесконфликтность (в том числе иммунологическую) широко распространенного носительства потенциально опасного агента.
Возбудитель сифилиса
Наглому дай волю, он захочет и боле.
Кто знает сифилис, знает медицину.
В. Ослер
- Трепонемы и бледная спирохета.
- Неудачи культивирования.
- Первичная инвазия.
- Клиническая и микробиологическая эволюция процесса.
- Врожденный сифилис.
- Иммунология и иммунопатогенез.
- Парадоксы иммунодиагностики.
- Сальварсан и антибиотики.
Сифилис относится к классическим заболеваниям, передаваемым половым путем. Его изучение занимает заметное место в истории микробиологии, иммунологии и химиотерапии. После недолгого затишья сифилитическая инфекция вновь получила широкое распространение. Ее патогенез остается загадкой. Достоверно известны лишь несколько стадий, которые удивительно многолики и клинически не похожи друг на друга. Две первые из них (первичный и вторичный сифилис) протекают как острое и подострое заболевания, третичный сифилис — хроническая болезнь, которая продолжается много лет и никогда не завершается самоизлечением. Сифилис может заявить о себе в любом возрасте, так как его возбудитель, Treponema pallidum, передается от матери плоду и годами сохраняется в организме, часто в латентном (точнее псевдолатентном) состоянии. Он не культивируется на искусственных питательных средах, и мало известно о факторах, которые определяют его патогенность и способность ускользать от иммунологического надзора. К счастью, T. pallidum сохраняет высокую чувствительность к антибиотикам. Поэтому современный сифилис хорошо поддается лечению, если процесс не достиг необратимых органических поражений.
Название болезни возникло в ХVI столетии, когда в Европе бушевала эпидемия сифилиса. В 1530 г. итальянец Джироламо Фракасторо, много и плодотворно размышлявший о природе заразных болезней, опубликовал поэму, повествующую о судьбе юного пастуха Сифилоса (Syphilos), заболевшего «венерической оспой». Примерно в это же время не менее знаменитый французский врач, математик и астроном Жан Фернель «окрестил» ту же болезнь Lues Venerea, чумой возлюбленных (от лат. lues — чума). С тех пор «сифилис» и «люис» используются как равноправные термины.
Микробиология. В естественных условиях сифилисом болеет только человек. Возбудитель относится к спирохетам — семейству бактерий с уникальной морфологией и структурой. Это спиралевидные, тонкие, гибкие, довольно длинные (до 20 мкм) клетки с активной подвижностью. Спирохеты широко распространены в природе, хотя лишь немногие из них вызывают болезни у человека и животных. Патогенные спирохеты принадлежат к трем родам — Treponema (сифилис, фрамбезия, пинта, беджел), Borrelia (возвратный тиф, болезнь Лайма) и Leptospira (лептоспироз).
Все трепонемы похожи друг на друга, и есть мнение, что они являются вариантами одного вида — T. pallidum, возбудителя сифилиса. Об этом говорит не только их структурное и физиологическое сходство, но и клиническая однотипность трепонемозов. Это хронические инфекции, которые могут продолжаться десятки лет с чередованием обострений и скрытых (латентных) периодов. В отличие от сифилиса, распространенного повсеместно, фрамбезия, пинта и беджел встречаются главным образом в тропических странах и протекают относительно доброкачественно.
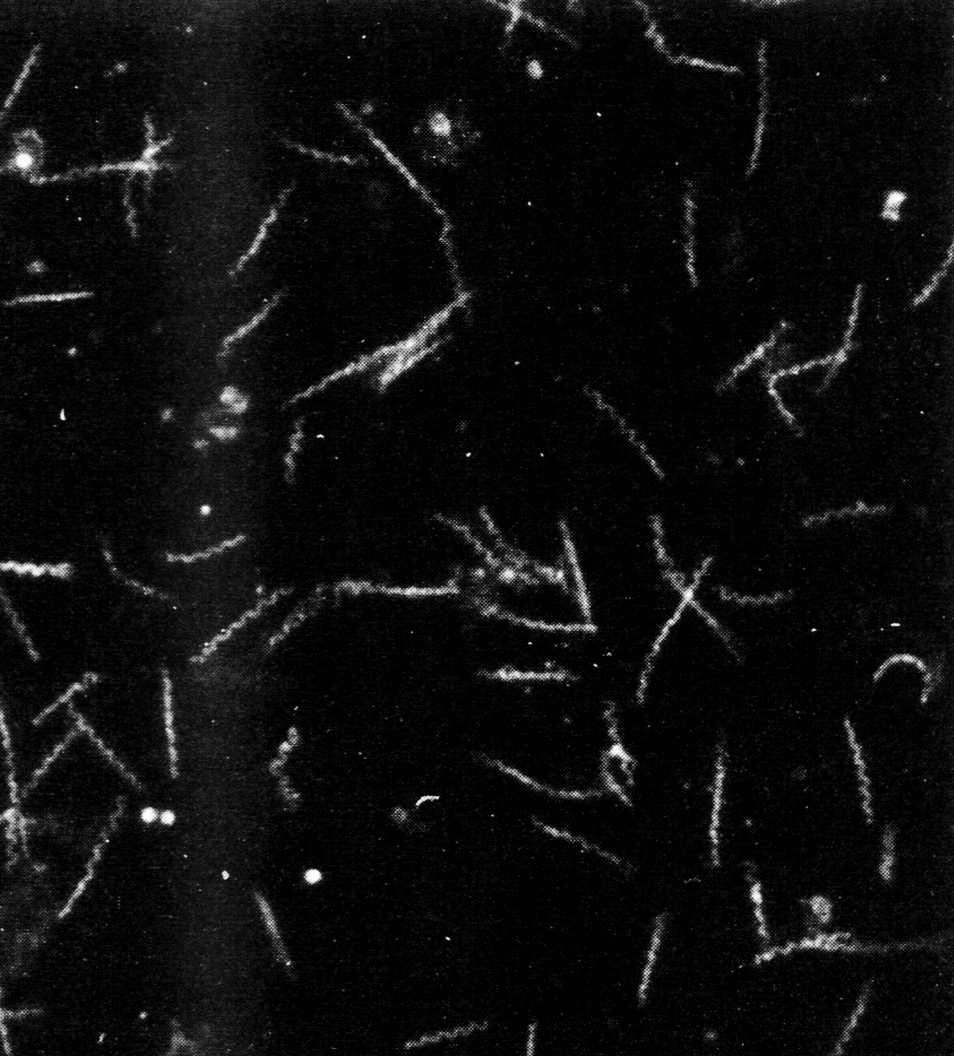
Возбудитель сифилиса открыт в 1905 г. Ф. Шаудином и Э. Гоффманом в экссудате тканей, пораженных сифилисом. Он получил название бледной (pallidum) спирохеты, так как, обладая очень тонким телом (ширина клеток 0,1—0,2 мкм), слабо прокрашивается анилиновыми красителями и плохо заметен под обычным микроскопом. Его удается хорошо рассмотреть при помощи темнопольной микроскопии (рис. 1), а также после импрегнации серебром, которое, осаждаясь на клетках, увеличивает их диаметр. В свежеприготовленных темнопольных препаратах трепонемы отличаются характерными движениями: активно перемещаются в среде путем штопорообразного вращения и медленных скачков. Это сопровождается сгибанием клеток под прямым (и более) углом без потери спиралевидной формы. Такого рода сгибательные движения отсутствуют у других спирохет, что является дифференциальным признаком рода Treponema (лат. — сгибающаяся нить).