Содержание
Это отвечает задаче борьбы с антибиотикорезистентными микобактериями — важным объектом современной фтизиатрии. Сочетание нескольких препаратов необходимо не только для того, чтобы уничтожить различные тканевые субпопуляции бактерий, но и для того, чтобы воспрепятствовать выживанию антибиотикорезистентных клонов, возникающих в результате внутрипопуляционной изменчивости. К сожалению, полностью избежать этого едва ли возможно. В последние годы все более широкое распространение получают штаммы, устойчивые не только к монопрепаратам, но и сразу к нескольким агентам. Они эволюционируют в регионах, где высокая заболеваемость туберкулезом сочетается с неполноценной этиотропной терапией, способствующей отбору и закреплению лекарственноустойчивых мутантов. Лечение должно быть длительным — 9—12 мес. Быстрое прекращение бацилловыделения (иногда через 1—2 мес) обманчиво и не гарантирует полной элиминации возбудителя.
Клостридии
Друзья по жизни мы, враги мы по несчастью.
- Экология: стратегия и тактика.
- Смертельно опасные сапрофиты.
- C. perfringens: лидер гистотоксических клостридий.
- C. perfringens: пищевые инфекции.
- C. difficile: псевдомембранозный антибиотикозависимый колит.
- C. tetani: от раневой инфекции к нейроинтоксикации.
- С. botulinum: нейроинтоксикация без инфекции.
Род клостридий (Clostridium) включает более 80 видов облигатно анаэробных, спорообразующих, крупных (3—10х0,4—1,2 мкм), грамположительных, обычно подвижных (перитрихии), палочковидных бактерий. Споры (точнее эндоспоры) вызывают утолщение клеток, придавая им вид веретена (рис. 1). Отсюда и название — клостридии (греч. kloster — веретено). Неоднородность клостридий проявляется в морфологии спор и вегетативных клеток, в чувствительности к кислороду, устойчивости во внешней среде, в условиях спорообразования и метаболической активности. Являясь сапрофитами, освобождающими природу от мертвого органического материала (через процессы брожения и гниения), клостридии обладают неодинаковой болезнетворностью. Лишь немногие из них вступают в прижизненные контакты с человеком и животными, обладая условной патогенностью. Присутствие болезнетворных клостридий в кишечнике (в том числе человека) не может поколебать отношения к ним как к сапрофитам: здесь они тоже питаются органическими остатками, не инвазируя живой ткани. Следует скорее говорить о том, что клостридии охотно меняют независимый образ жизни на симбиоз, перекладывая на хозяина заботы о взаимоотношениях с внешней средой. Оказавшись на свободе, они не только выживают в виде спор, дожидаясь очередной вегетации в организме хозяина, но и активно размножаются.
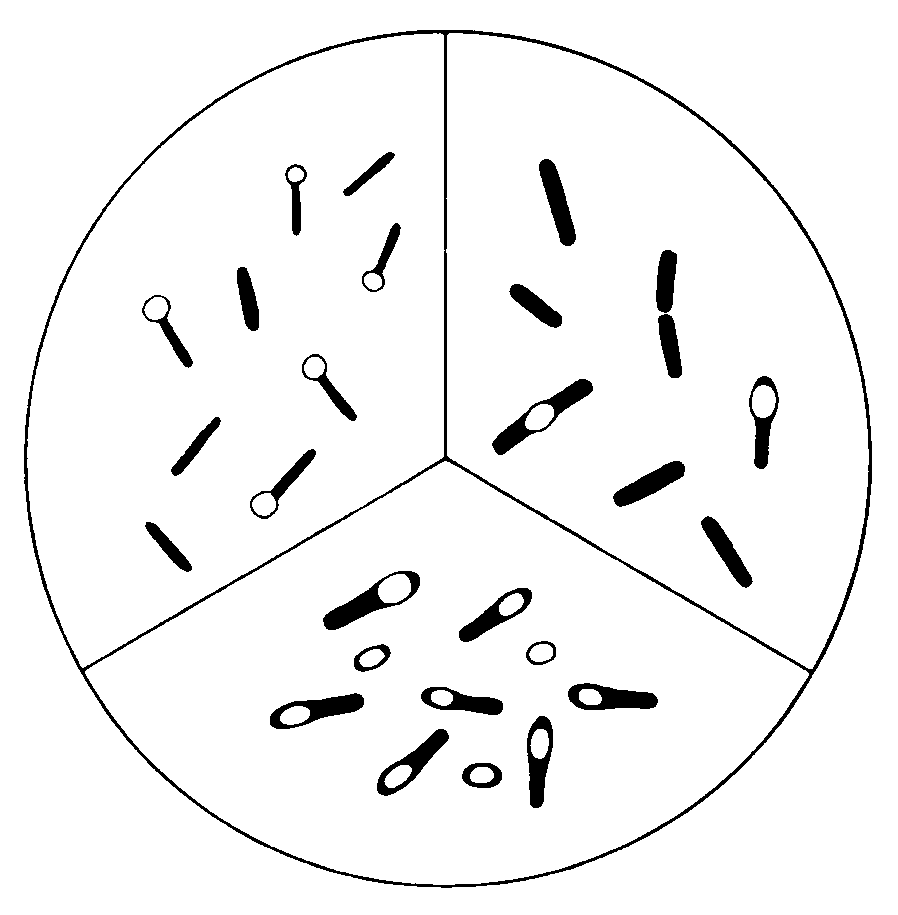
Являясь сапрофитами, освобождающими природу от мертвого органического материала (через процессы брожения и гниения), клостридии обладают неодинаковой болезнетворностью. Лишь немногие из них вступают в прижизненные контакты с человеком и животными, обладая условной патогенностью. Присутствие болезнетворных клостридий в кишечнике (в том числе человека) не может поколебать отношения к ним как к сапрофитам: здесь они тоже питаются органическими остатками, не инвазируя живой ткани. Следует скорее говорить о том, что клостридии охотно меняют независимый образ жизни на симбиоз, перекладывая на хозяина заботы о взаимоотношениях с внешней средой. Оказавшись на свободе, они не только выживают в виде спор, дожидаясь очередной вегетации в организме хозяина, но и активно размножаются.
Клостридии вызывают три смертельно опасных заболевания — газовую гангрену (C. perfringens и другие гистотоксические клостридии), столбняк (C. tetani) и ботулизм (C. botulinum). Кроме того, они причастны к патологии пищеварительного тракта, включая относительно доброкачественные энтероколиты и деструктивные процессы, требующие активного врачевания (С. perfringens, C. difficile). Патогенность связана со способностью продуцировать мощные токсины, которые образуются в инфицированном организме или во внешней среде (C. botulinum). Инвазивность почти всегда ограничена, и даже при массивных поражениях (газовая гангрена) носит вторичный характер, следуя за анаэробным повреждением тканей. Не случайно о клостридиях говорят как о некропаразитах, подчеркивая их неспособность к размножению в живых, хорошо снабжаемых кровью тканях.
Clostridium perfringens
Подобно другим клостридиям, C. perfringens (син. С. welchii) широко распространены во внешней среде, особенно в унавоженных почвах. Они сохраняются здесь не только в виде спор, но и активно вегетируют, особенно при повышенной (45°С) температуре. Вместе с тем представители этого вида, пожалуй, больше, чем другие клостридии, экологически связаны с кишечником человека и животных. У человека они определяются в количестве 103—105 бактерий на 1 г фекалий (для сравнения: содержание факультативно-анаэробных бактерий, прежде всего кишечной палочки и энтерококков, составляет 106—107/г, а бактероидов и бифидобактерий, доминирующих в кишечном микробиоценозе, — 109—1010/г).
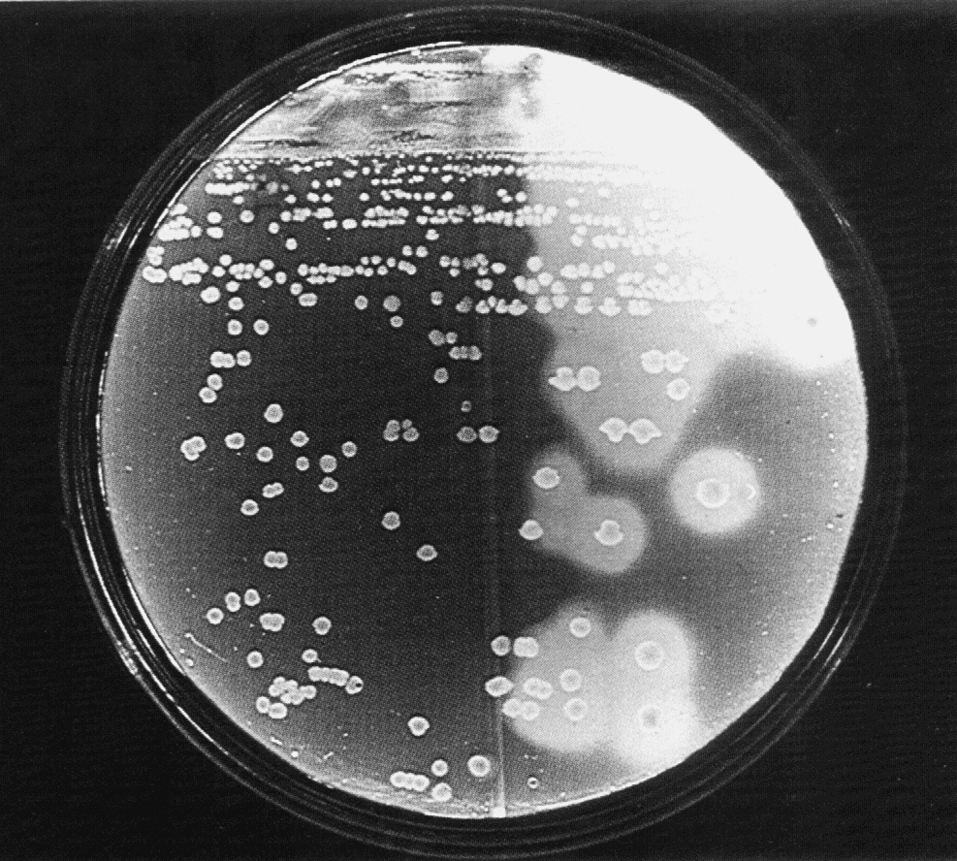
Видовой эпитет (perfringens) означает «прорывающий», «разламывающий». Он отражает мощную ферментативную активность данного вида клостридий, которые благодаря энергичному газообразованию разрывают питательные среды и столь же активно ведут себя в инфицированных тканях (рис. 2).

По спектру продуцируемых токсинов различают пять типов C. perfringens — A, B, C, D, E. Заболевания человека чаще связаны с типом А (газовая гангрена, пищевые инфекции) и изредка — С (некротизирующий энтероколит). В целом понятие «токсин» у C. perfringens довольно расплывчато. Оно объединяет не менее 14 факторов с летальной и гистолитической активностью. Главными являются альфа-, бета, эпсилон- и йота-токсины. Именно их комбинация определяет тип C.perfringens. Альфа-токсин продуцируют только клостридии типа А. Это мощный цитотоксин, обладающий свойствами фосфолипазы С. Он расщепляет фосфолипиды (лецитин) клеточных мембран, лизируя клетки (рис. 3).
При газовой гангрене альфа-токсин служит не только главным эффектором внутритканевой инвазии, но и причиной внутрисосудистого гемолиза — символа смертельной клостридиальной токсинемии. Из других (минорных) токсинов C. perfringens типа А образует тета-токсин, или перфринголизин (чувствительный к кислороду гемолизин, похожий на О-стрептолизин стрептококка), каппа-токсин (коллагеназа), мю-токсин (гиалуронидаза) и ню-токсин (ДНК-аза). Они лишены самостоятельного значения, но усиливают действие альфа-токсина.
Штаммы типа А, вызывающие пищевое отравление, продуцируют энтеротоксин. Это термолабильный белок с молекулярной массой 35 кДа, который высвобождается в тонком кишечнике при споруляции (образовании спор). Подобно энтеротоксинам холерного вибриона и энтеробактерий, он усиливает секрецию энтероцитами Na+, Cl— и воды, но достигает этого иным путем: он не повышает внутриклеточного уровня цАМФ, а повреждает плазматическую мембрану энтероцитов. Это единственный такого рода пример среди диареегенных бактерий. Особняком стоит энтеропатогенность C. perfringens типа С. Она связана с бета-токсином и проявляется в виде некротизирующего энтерита (см. ниже).