Содержание
Как уже говорилось, 70-килобайтовой плазмидой обладают вирулентные штаммы всех трех видов иерсиний (Y. pestis, Y. psedotuberculosis и Y. enterocolitica) и все они обладают способностью к продукции Yops. Но оказалось, что этот признак тоже зависит от экологии, максимально проявляясь при 37°С в отсутствие внеклеточного Са2+ (отсюда название ряда наружных белков, контролирующих секрецию III типа — Lсr, от англ. low-calcium response). Секреция III типа — контактный феномен, который зависит от взаимодействия бактерий и эукариотических клеток и именно это является причиной реакции в условиях инфекционного процесса. Внедрившиеся в организм иерсинии проявляют агрессивность, находясь вне клеток. Этому способствует устойчивость к компонентам сыворотки, прежде всего к комплементу, которая определяется наружными белками, в частности Ail и YadA (у Y. pestis — капсульный протеин F1).
К тому, что было сказано о факторах патогенности иерсиний (Y. pseudotuberculosis и Y. enterocolitica), можно добавить информацию о дискуссии об энтеротоксине, который по механизму действия близок (если не идентичен) термостабильному энтеротоксину кишечной палочки. Сомнения относительно его патогенетических функций связаны с тем, что он почти не образуется при 37°С. Кроме того, авирулентные штаммы, лишенные плазмиды, где закодированы белки патогенности, способны продуцировать энтеротоксин, не вызывая патологии.
Много внимания уделяется иерсиниозным сидерофорам — белкам, конкурирующим за ионы железа. Допускают даже, что одним из условий, предрасполагающих к генерализации иерсиниоза, служит избыток свободного железа в организме, например при гемолитической анемии.
В целом, иерсинии следует отнести к числу наиболее многогранных патогенов. Обладая набором факторов, детерминируемых хромосомными и плазмидными генами, они являются великолепным примером бактерий, способных рационально перестраивать свой фенотип в зависимости от обстановки, добиваясь внедрения в интимные сферы гомеостаза хозяина. Это отличная модель для изучения молекулярных механизмов экологически зависимой пластичности бактерий в проекции на вполне утилитарные проблемы эпидемиологии и инфекционной патологии.
Возбудители холеры
Сто друзей — мало, один враг — много.
- Условия проявления болезнетворности холерного вибриона.
- История холерных эпидемий.
- Микробиология и серология холерного вибриона.
- Факторы вирулентности, патогенез и клиника холеры.
- Экология холерного вибриона и эпидемиология холеры.
- Лабораторная диагностика, лечение и проблемы специфической профилактики холеры.
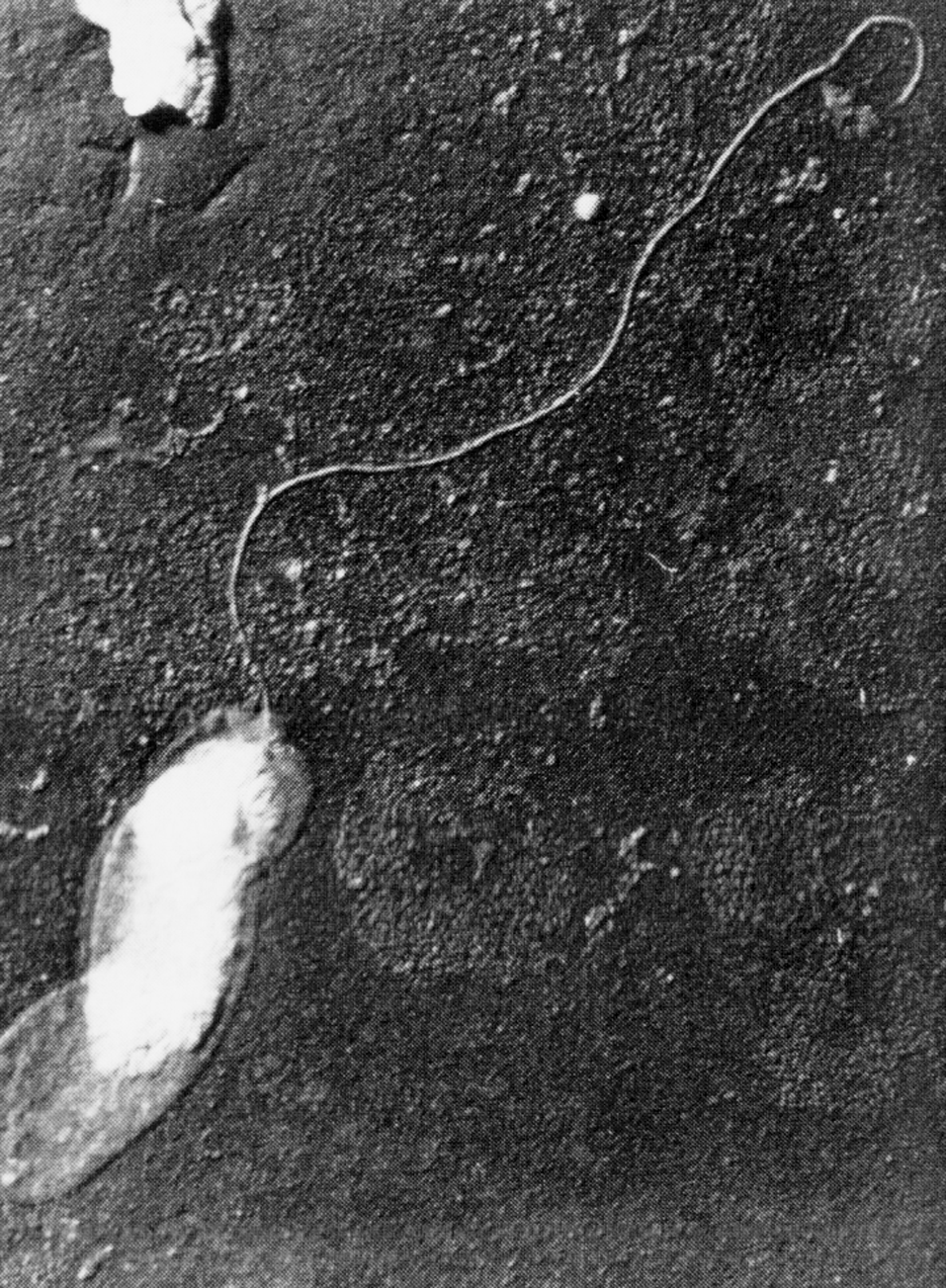
Холерный вибрион принадлежит к роду Vibrio семейства Vibrionaceae. Сюда же относятся еще два рода, занимающих определенное место в медицинской микробиологии — Aeromonas и Plesiomonas. Все они являются бактериями с полярным жгутиком (рис. 1), живут в свежей или морской воде, в кишечнике животных и человека. Из более чем 30 видов рода Vibrio особое значение имеет Vibrio cholerae.
Холера — острая кишечная инфекция, вызываемая энтеротоксинпродуцирующими штаммами холерного вибриона. Она протекает в разных вариантах — от бессимптомного инфицирования до тяжелого процесса с внезапной профузной диареей, ведущей к гиповолемическому шоку, ацидозу и смерти. Это антропоноз, поражающий только человека; мишенью для возбудителя служат энтероциты тонкого кишечника. Здесь холерные вибрионы находят оптимальные условия для быстрого размножения (щелочная среда, продукты переваривания белков) и даже вытесняют другие микробы.
Вибрион поступает в кишечник через кислую среду желудка, которая служит для него мощным барьером. Являясь ацидочувствительным, он преодолевает эту преграду только при массированном заражении (106 токсигенных вибрионов не вызывают симптомов у взрослых добровольцев, если они принимаются без пищи), хотя реальная заражающая дозировка может быть ниже. Вибрионы ускользают от действия соляной кислоты не только при нарушениях секреторной деятельности желудка (гипоацидный гастрит), но и при его нормальном функционировании. Это происходит, если холерный вибрион находится внутри пищевого комка (который защищает его от кислот) или при поступлении в желудок вместе с водой (особенно щелочной), которая быстро выбрасывается в кишечник, снижая концентрацию соляной кислоты. При приеме тех же токсигенных вибрионов в количестве 106 вместе с пищей развитие холеры наблюдали у 80—100% добровольцев. Тщательные микробиологические исследования, проведенные в Бангладеше, показывают, что клинически значимая дозировка V. cholerae составляет 102—104 клеток. Опыты на добровольцах, которые проводились на фоне подавления кислотности желудка бикарбонатом натрия, в целом подтверждают эти наблюдения. Диарейная болезнь у большинства субъектов развивалась после приема 103—104 холерных вибрионов, но заболевание протекало менее тяжело, чем от более высоких дозировок.
Холера известна с незапамятных времен. Она возникла в Южной Индии, в низовьях рек Ганга и Брахмапутры, т.е. на территории, сегодня известной как государство Бангладеш. До начала ХIX столетия холера оставалась эндемичной для данного региона, и только в 1817 г. с развитием миграции населения и расширением людских контактов произошло распространение инфекции на соседние регионы и отдаленные страны, включая Европу и Америку. Холера стала пандемически опасной болезнью, борьба с которой требует огромных средств. Ежегодные вспышки уносят жизнь около 120000 человек, но еще больше людей страдает от тяжелых форм холеры. Строгое соблюдение гигиенических мер безопасности, основанных на знании экологии возбудителя, ограничивает распространение холеры регионами Индостана, Южной Азии, Африки и Латинской Америки. Однако с опасностью заноса холеры приходится считаться всем странам, включая Россию. Не случайно холеру называют в числе «вновь появляющихся» инфекций (emerging and reemerging infections), угрожающих многим развивающимся странам.
С 1817 г. человечество знало восемь пандемий холеры, унесших (и продолжающих уносить) огромное число человеческих жизней. Во время пятой из них, в 1883—1884 гг., Р. Кох изолировал ее возбудителя, V. cholerae, который сегодня отнесен к биотипу «классический». В 1961—1962 гг. началась новая, седьмая по счету пандемия холеры, вызванная другим биотипом V. cholerae О1 — Эль-Тор. Он вырвался за пределы своего эндемичного очага на острове Сулавеси в Индонезии и обычным путем, через государства Юго-Восточной Азии, охватил Средний Восток, африканские страны, южные районы бывшего СССР и даже достиг Европы (Португалия, Испания, Франция), Америки и Японии. Пандемия прекратилась к 1993 г., оставив после себя новые очаги эндемичной холеры в Азии и Африке. В 1962 г. ВОЗ признал инфекцию, обусловленную вибрионом Эль-Тор, холерой, включив ее в группу карантинных заболеваний. Это произошло всего через четыре года после заявления о том, что холера исчезает, а инфекцию Эль-Тор нельзя считать холерой.
В 1992—1993 гг. в Индии и Бангладеше зарегистрирована эпидемия «новой» холеры, вызванной штаммом О139 V. cholerae. С тех пор вспышки холеры О139 появлялись в Пакистане, Афганистане, Непале, Китае, Таиланде и других странах, соседствующих с первоначальным очагом. На этот раз ВОЗ поступила осторожнее, быстро признав в V. cholerae О139 возбудителя холеры с пандемическим характером распространения.
Итак, возбудителями современной холеры являются представители серогруппы О1 (V. cholerae, биотип classiс и V. cholerae, биотип El-Tor, почти вытеснивший первого из них) и О139 (V. cholerae O139, син. Bengal). Вариант Эль-Тор отличается от классического биотипа по своей гемолитической активности (гемолиз бараньих эритроцитов) и резистентности к полимиксину В. Их можно дифференцировать также по чувствительности к специфическим фагам.