Содержание
Подобно всем клостридиям, C. difficile убиквитарен, персистируя в почве, воде и кишечном содержимом многих животных. Вместе с тем возбудитель редко (всего в 3% случаев) выделяется из фекалий здоровых взрослых людей. Носительство возрастает у госпитальных больных (13—30%), отражая обмен микрофлорой при плотных контактах. Отсюда возникает комплекс мероприятий, направленных на предупреждение заражения, особенно в больницах, где уже отмечались вспышки инфекции. Парадоксом является широкая контаминация здоровых детей — 14—50%; у новорожденных она достигает даже 90%. Полагают, что токсины C. difficile не рецептируются энтероцитами новорожденных и не вызывают их поражения.
События, ведущие к диарейному синдрому, начинаются с антибиотикозависимого подавления нормальной микрофлоры, прежде всего анаэробных неспоровых бактерий (бактероидов, бифидобактерий), — основы колонизационной резистентности толстого кишечника. Наиболее опасны антибиотики типа клиндамицина, которые, обладая высокой активностью против анаэробных бактерий, длительно (до 5 дней) сохраняются в кишечнике после однократного приема. C. difficile выживают благодаря образованию спор. Прорастая после отмены антибиотиков, они дают начало обильному потомству вегетативных клеток, продуцирующих токсины.
C. difficile образует два главных токсина — А и В. Они секретируются большинством штаммов, обладая неодинаковым спектром биологической активности, закодированной вместе с позитивным и негативным регулятором в острове патогенности (см. «Болезнетворность бактерий»). Это наиболее крупные (308 и 269 кДа) из однонитевых бактериальных экзотоксинов, которые имеют до 45% сходства в последовательности аминокислот. Рецепторы известны только для токсина А.
В состав токсинов А и В входит каталитический домен, определяющий глюкозилирование G-белков — Rho, Rac и Cdc42. Это лишает G-белки ферментативной способности к трансформации ГДФ—ГТФ, от которой зависят многие важные функции клеток, в том числе полимеризация-деполимеризация актина. Токсин А действует как энтеротоксин. Повреждая мукозальные клетки, он вызывает образование вязкой кровянистой жидкости в просвете изолированной кишки кролика. Агрессивность токсина В более универсальна. В культуре клеток он в 1000 раз токсичнее, чем токсин А, приводя к округлению клеток благодаря повреждению цитоскелета. Антитоксический иммунитет, который удается воспроизвести на животных, клинически не надежен, так как токсины быстро связываются чувствительными клетками, ускользая от нейтрализующих антител. Выявление токсинов в фекалиях рекомендовано для подтверждения клинического диагноза. Это много проще, чем выделение и идентификация культуры C. difficile.
Лечение нацелено на уничтожение вегетирующих клеток C. difficile. Эффективны метронидазол и ванкомицин, которые благодаря плохой всасываемости при пероральном приеме накапливаются в толстом кишечнике. Проблемой остаются рецидивы, поскольку антибиотики не гарантируют полного освобождения кишечника от спор и даже способствуют их образованию. В связи с этим логичным выглядит восстановление нормального микробиоценоза при помощи пробиотиков, т.е. живых нормальных бактерий толстого кишечника. Положительный опыт такого рода экспериментально обоснован, но клиническая значимость современных препаратов (на основе бифидобактерий, лактобацилл, кишечной палочки) сомнительна. Определенные надежды связывают (и уже пытаются реализовать) с дрожжами Saccharomyces boulardii, которые не очень понятным образом тормозят размножение C. difficile и образование их токсинов в кишечнике. Есть данные, говорящие о том, что S. boulardii выделяют протеазу, разрушающую клостридиальные токсины, или действуют как фактор, блокирующий транскрипционные процессы в эпителиоцитах, необходимые для передачи токсигенных сигналов С. difficile.
Clostridium tetani
Первые описания столбняка (tetanus) встречаются у Гиппократа и других врачей древности. Инфекционная природа заболевания экспериментально обоснована Карлэ и Раттом в 1884 г. Остроумные опыты (1884—1886 гг.) провел Николайер. Он показал, что инокуляция взвеси почвы вызывает столбняк у животных. Обнаружив в зоне инъекции длинные, тонкие палочки, отсутствовавшие в других тканях, Николайер предположил, что возбудитель размножается местно, продуцируя стрихниноподобный яд — непосредственную причину болезни. Розенбах (1886—1887 гг.) подтвердил наблюдения Николайера, выявив у столбнячных больных спорообразующие палочки. Круг сомкнулся, когда Китазато (1889 г.) воспроизвел столбняк при введении животным чистой культуры возбудителя. Перед анаэробным культивированием раневого содержимого от больного столбняком он догадался уничтожить неспоровые бактерии, подвергнув исследуемый субстрат термической обработке.
Характерным морфологическим признаком столбнячных бацилл являются круглые терминальные споры, благодаря которым они выглядят как булавки или барабанные палочки (рис. 6).
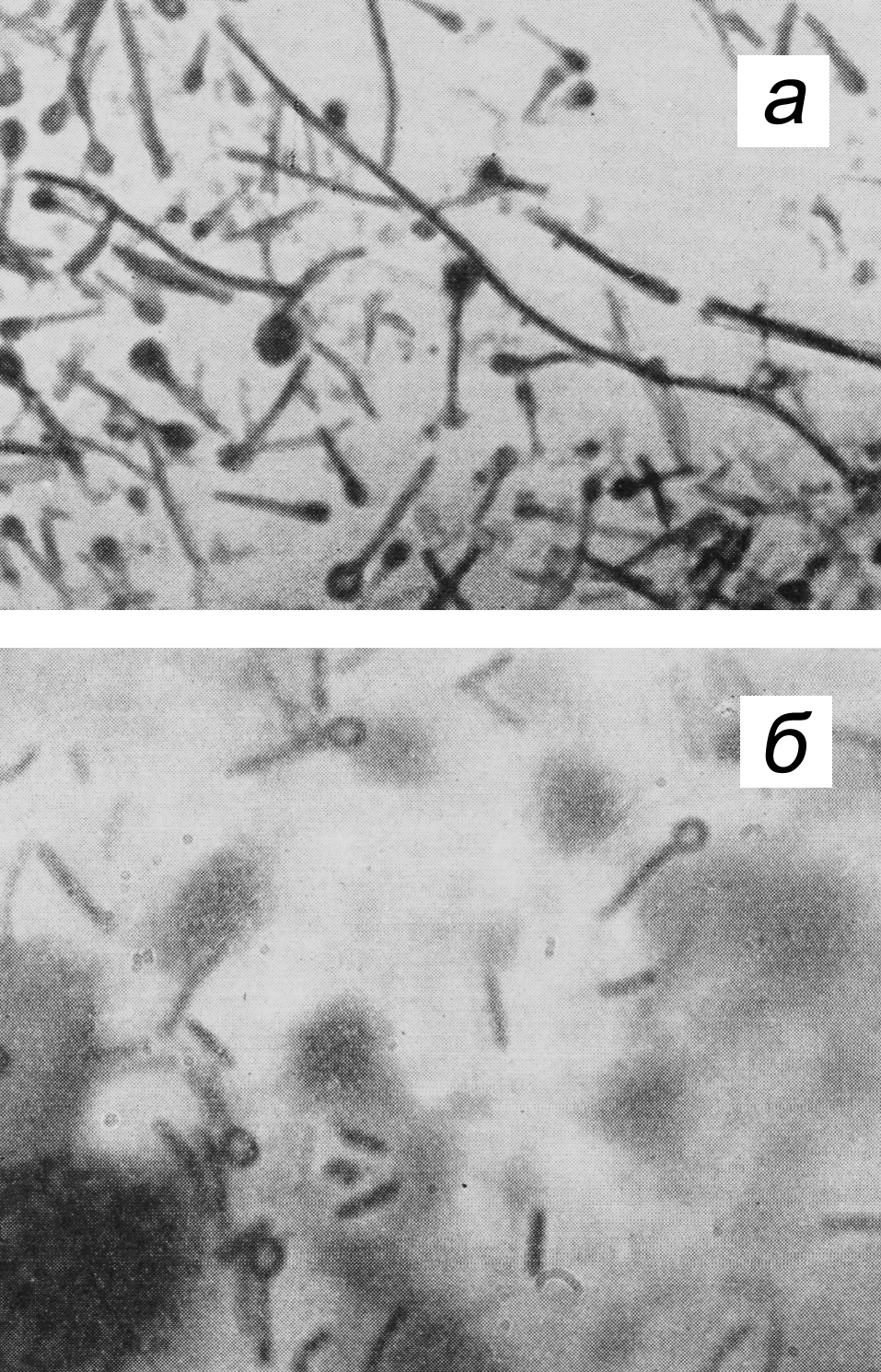
В культурах споры образуются через несколько суток и, по разным данным, переносят кипячение от 20 мин до 3 ч. Столбнячные палочки подвижны и по антигенным особенностям жгутиков подразделяются по меньшей мере на десять серотипов. Впрочем, это не имеет практического значения, так как все разновидности C. tetani вырабатывают идентичный нейротоксин, что обеспечивает единство патогенеза и унификацию иммунопрофилактики.
Клостридии столбняка широко распространены в природе, прежде всего в почве, особенно на возделываемых (окультуренных) участках. Нередко они обнаруживаются и в кишечнике человека и животных, хотя стиль их жизни в этом случае остается загадкой. Возможно, столбнячные бациллы здесь не размножаются, проходя транзитом в виде спор. Не исключена и вегетация, о чем говорят следы противостолбнячного антитоксина в сыворотке здоровых животных. Но если это и так, столбняк никогда не возникает при всасывании токсина из кишечника, тем более что вызвать заболевание путем перорального введения токсина не удается.
Столбняк развивается как раневая инфекция, но далеко не каждое ранение создает условия для прорастания спор и размножения бактерий. C. tetani принадлежит к числу наиболее строгих анаэробов, и во многих случаях это спасает от фатальных последствий. Глубокая гипоксия, необходимая для токсинообразования, как правило, возникает в зоне некроза, и все, что было сказано о возбудителях газовой гангрены, справедливо для cтолбнячных клостридий. Однако, отмечая опасность тяжелых травм, следует помнить, что даже малые повреждения могут стать причиной столбняка. Коварны колотые раны (от гвоздей, заноз, колючек и пр.), в глубине которых возникает анаэробиоз. Не случайно у 20% больных отсутствуют указания на травму. Это не означает, что ее не было. Просто она не запомнилась из-за незначительности. Есть подозрения, что столбнячные споры могут персистировать в тканях. По крайней мере известны случаи столбняка, спровоцированные локальной ишемией спустя более 10 лет после предполагаемого заражения. У новорожденных инфекция проникает через пупочный канатик, так что tetanus neonatarum (рис. 7) остается реальностью в странах с низкой санитарной культурой и плохо налаженной иммунопрофилактикой. Беременные женщины должны вакцинироваться столбнячным анатоксином, чтобы обеспечить пассивный иммунитет новорожденных.
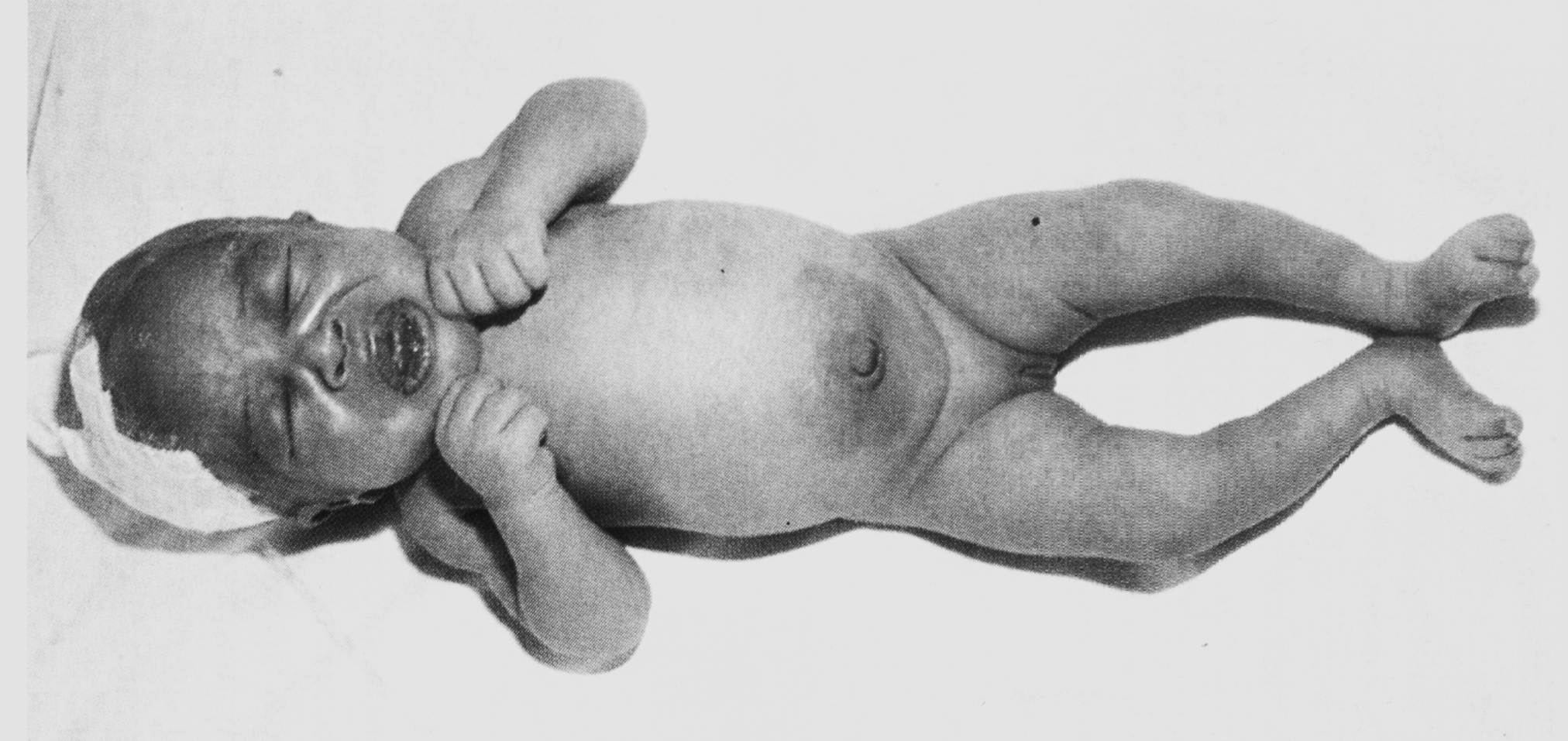
В отличие от гистотоксических клостридий, C. tetani лишен инвазивности (возбудитель не покидает места первичного заражения), и заболевание всегда протекает как интоксикация на фоне малосимптомной очаговой инфекции. Столбнячный нейротоксин называется тетаноспазмином, что подчеркивает ведущий, по сути единственный патогенетический механизм столбняка — спастические параличи поперечно-полосатых мышц. Столбнячный токсин принадлежит к классике микробной токсинологии, уступая по биологической активности только ботулиническому яду. Вслед за человеком к нему наиболее восприимчивы лошади, белые мыши и морские свинки. Птицы и хладнокровные животные резистентны к столбняку. Смертельная доза для мыши составляет всего 3·10-11 г, т.е. 1 мг достаточно, чтобы убить 50—70 млн. мышей.