Содержание
Сальмонеллы должны пройти сквозь пищеварительный тракт, чтобы оказаться в зоне, оптимальной для своей первичной колонизации — дистальном отделе подвздошной кишки. Это ведет к большим потерям бактерий, так как сальмонеллы значительно чувствительнее к кислой среде желудка, чем, например, шигеллы. Клинически значимая доза S. typhimurium при нормальной кислотности желудка составляет 10—100 млн. бактериальных клеток, в то время как та же дозировка в смеси с нейтрализующим кислоту бикарбонатом натрия снижается в 10—100 раз.
Сальмонеллы располагают генами, среди которых следует отметить двухкомпонентную систему PhoP/PhoQ. Это глобальный регулятор вирулентности, который улавливает в окружающей среде различные сигналы (в том числе рН), приводя к транскрипционному включению или выключению более 40 генов. Динамическое изменение экспрессии этих и других генов позволяет бактериям лучше адаптироваться к меняющимся условиям внешней среды, проявляя свою вирулентность.
Сальмонеллы прикрепляются к энтероцитам с помощью комплекса хромосомных и плазмидных адгезинов, оформленных в виде пилей, и, подобно шигеллам, пенетрируют мукозальный барьер. Нельзя с уверенностью сказать, какие структуры при этом вовлекаются, так как все типы эпителиальных клеток чувствительны к инвазии сальмонелл. Тем не менее все больше данных говорит о том, что местом первичной колонизации служат М-клетки, покрывающие лимфоидные агрегаты. Ангажируя этот маршрут, сальмонеллы проходят к макрофагам, располагающимся под ними. Феномен связан с продуктами инвазивных генов (invA-E), которые внедряются в клетку при помощи аппарата контактной секреции III типа. Расположенные в острове патогенности (SPI-1), они влияют на цитоскелет хозяйской клетки, вызывая эндоцитоз бактерий путем раффления (англ. ruffling — волнение, рябь) ее плазматической мембраны. Это указывает на цитоскелетную перестройку, приводящую к формированию мембраносвязанной везикулы (рис. 1). Проникновение сальмонелл в клетки является примером микробзависимого фагоцитоза.

В отличие от шигелл, которые для размножения должны быстро выйти в клеточную цитоплазму, сальмонеллы многие часы остаются внутри фагосом. Через 6—24 ч в эпителиальных клетках большие вакуоли, заполненные бактериями, перемещаются к базальной мембране, освобождая сальмонеллы в основную пластинку (lamina propria) и подслизистый слой. Это сопровождается восстановлением поверхностных структур (микроворсинок) клеток и их стимуляцией к секреции интерлейкина-8 и других провоспалительных цитокинов. Аккумуляция нейтрофилов ведет к продукции простагландинов, которые в значительной степени отвечают за усиление секреции жидкости (диарею) мукозальными клетками. Можно сказать, что для сальмонелл интестинальные эпителиоциты, не являясь главной средой для размножения, служат скорее барьером, который им надлежит преодолеть. При выходе из эпителия сальмонеллы захватываются макрофагами. Испытывая микробное давление (в частности, действие продуктов SPI-1 на каспазу-1), они выделяют дополнительные порции провоспалительных цитокинов, подвергаясь апоптозу. Пребывание в фагоцитах требует от сальмонелл участия более 40 новых генов (хромосомных и плазмидных); не меньшее число генов подлежит отключению. В конечном счете верх берут защитные силы хозяина, который оказывается сильнее бактерий. Инвазия «местных» (энтеритпродуцирующих) сальмонелл практически заканчивается на этом этапе. Лишь изредка некоторые штаммы (возможно, биовары) проникают в сосудистое русло, вызывая генерализованные процессы с развитием септикопиемических состояний.
Впрочем, есть наблюдения, позволяющие усомниться в значимости интестинальной инвазии для «местных» сальмонелл. Выявлено, в частности, что для индукции энтерита необходимы лишь эффекторные белки внеклеточных бактерий. Кроме того, установлено, что различные серотипы, которые равноценно инвазируют интестинальные эпителиоциты, отличаются по энтеропатогенности. Наконец, не исключено, что некоторые сальмонеллы все-таки продуцируют энтеротоксины, меняющие кишечный транспорт электролитов и воды. Дополнительные исследования должны внести ясность в эту проблему, но пока приходится принять за основу концепцию об инвазивно-воспалительном генезе сальмонеллезной патологии.
С лабораторными целями производят культуральный анализ испражнений больного, сопоставляя его результат с данными исследования подозреваемого источника заражения. Финалом анализа является определение антигенной формулы выделенного возбудителя.
Брюшной тиф/паратифы
Иначе обстоит дело с сальмонеллами (S. typhi, S. paratyphi A, B и С), вызывающими брюшной тиф и паратифы — близкие по клинике и эпидемиологии заболевания. Это антропонозы, единственным источником которых является человек — больной или (чаще) бактерионоситель, загрязняющий фекалиями окружающую среду. Наибольшее значение имеют зараженные молоко (в меньшей степени — другие продукты питания) и вода; передача контактно-бытовым путем встречается редко.
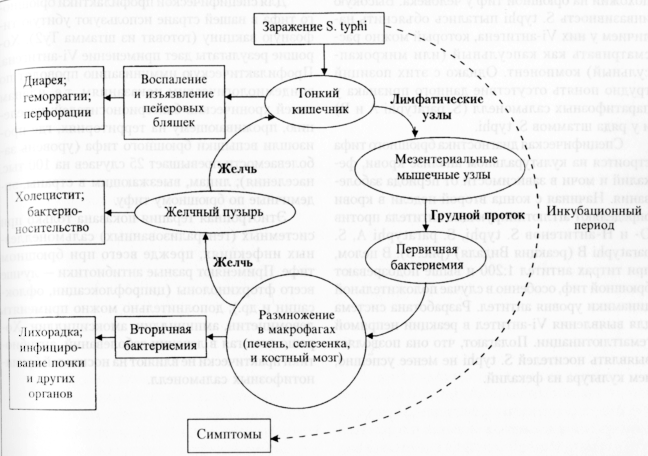
После перорального приема патогенетически значимой дозировки возбудитель доходит до тонкого кишечника и поначалу ведет себя как «местные» сальмонеллы. Он инвазирует интестинальный эпителий, переходя в основную пластинку (lamina propria) и подслизистую оболочку, где поглощается мононуклеарными фагоцитами. С этого момента его судьба принимает иной оборот: кишечная инфекция превращается в генерализованную инвазию. Сальмонеллы переносятся в регионарные (мезентериальные) лимфоузлы, после размножения попадают в грудной лимфатический проток и далее в кровяное русло (первичная бактериемия). Микробы быстро захватываются фиксированными макрофагами печени, селезенки и костного мозга, продолжая здесь размножение с образованием гранулем и вызывая гибель макрофагов (возможно, от апоптоза). Высвобождение в кровь большого количества сальмонелл означает вторичную бактериемию и совпадает с началом серьезной клиники, т.е. знаменует окончание инкубационного периода, который в среднем продолжается 14 дней. Типичными симптомами на первой неделе являются высокая температура, головная боль, бред, нарушения сердечно-сосудистой системы и другие признаки тифозного состояния. Наблюдаются розеолезная сыпь, запор, редко диарея. Чаще всего сальмонеллы обнаруживаются (но не размножаются) в крови на протяжении первых 10 дней болезни. Это период, когда они непрерывно поступают сюда из тканей, разрушаются, высвобождая эндотоксин и вызывая синдром диссеминированной внутрисосудистой гемокоагуляции — возможно, основной патогенетический механизм брюшного тифа.
Начиная со второй недели сальмонеллы попадают из печени в желчный пузырь и отсюда с током желчи снова в тонкий кишечник. Болезнь обретает иные черты, хотя по-прежнему остается тяжелой. Процент позитивных гемокультур падает, но возрастает число копрокультур, в которых присутствует возбудитель. Сталкиваясь с сенсибилизированными Т-лимфоцитами пейеровых бляшек, сальмонеллы вызывают их стимуляцию с выделением макрофагактивирующих цитокинов, которые запускают уничтожение сальмонелл в аллергических реакциях замедленного типа. Это сопровождается повреждением тканей и возникновением язв вследствие отторжения некротических масс в центре групповых лимфатических и солитарных фолликулов. Возникает диарея («гороховый суп» с кислым запахом), которая в тяжелых случаях становится геморрагической. На третьей неделе может случиться перфорация тонкого кишечника — самая распространенная причина смерти от брюшного тифа. При неосложненном течении язвы заживают, температура постепенно снижается и больной поправляется на 4—5-й неделе (рис. 2).