Содержание
В большинстве случаев бактерии полностью элиминируются в процессе выздоровления. Однако у небольшого числа больных (2—5%) сальмонеллы остаются в желчном пузыре или (реже) в мочевыводящей системе. Половина таких людей превращаются в хронических носителей, постоянно выделяя возбудителей (чаще S. typhi) во внешнюю среду.
Безусловно, сказанное требует участия многих бактериальных генов и их продуктов. Но сегодня брюшной тиф и паратифы, бывшие когда-то весьма распространенными болезнями, встречаются редко. Это связано с расшифровкой экологии их возбудителей и разработкой методов борьбы с источниками и распространением заболевания. Большинство информации связано с наблюдениями за системой «S. typhimurium—мыши», в которой по не очень понятным причинам возникает системный процесс, похожий на брюшной тиф у человека. Высокую инвазивность S. typhi пытались объяснить наличием у них Vi-антигена, который можно рассматривать как капсульный (или микрокапсульный) компонент. Однако с этих позиций трудно понять отсутствие данного признака у паратифозных сальмонелл (S. paratyphi А и В) и у ряда штаммов S. typhi.
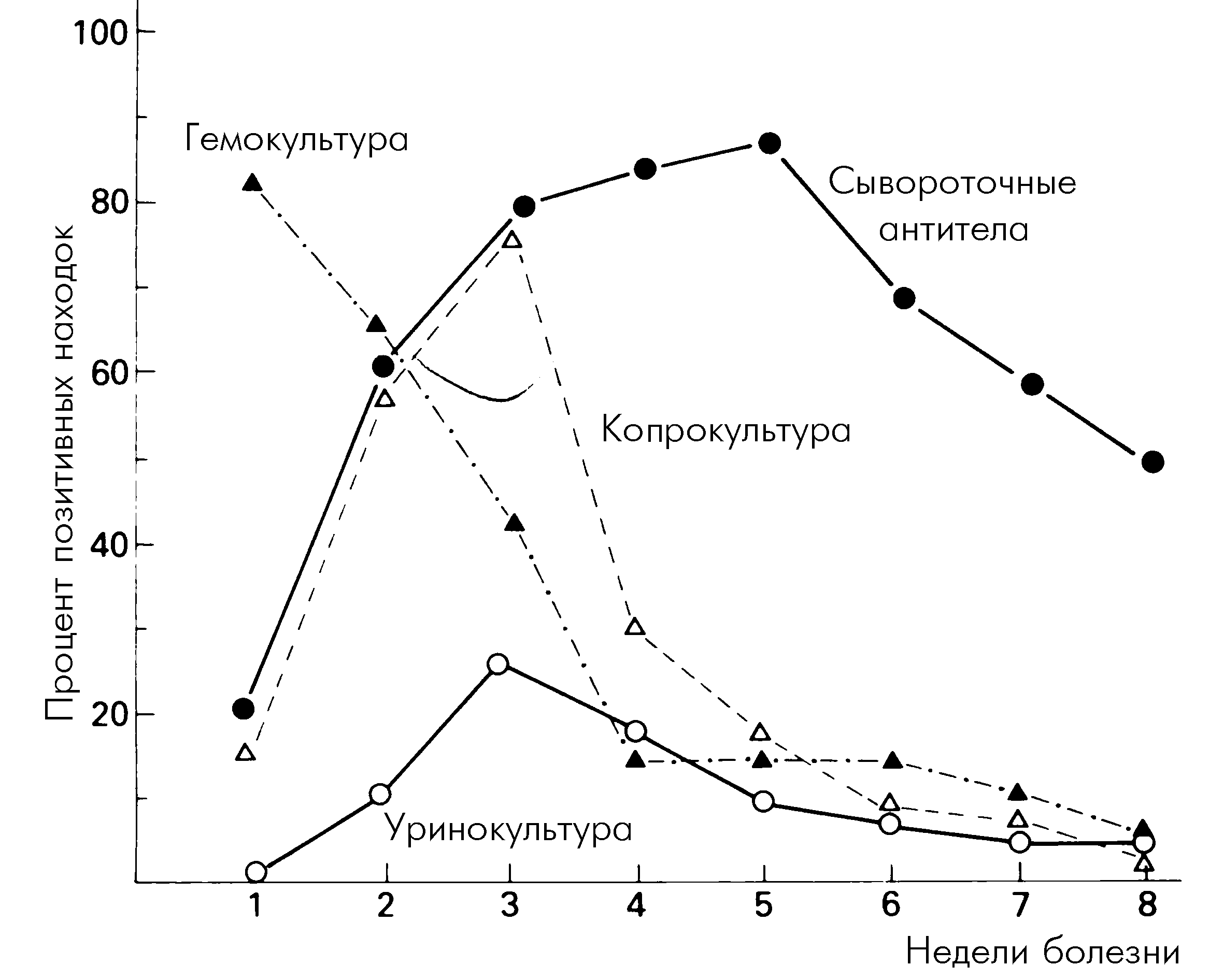
Специфическая диагностика брюшного тифа строится на культуральном анализе крови, фекалий и мочи в зависимости от периода заболевания. Начиная с конца второй недели в крови определяют агглютинирующие антитела против О- и Н-антигенов S. typhi, S. paratyphi A, S. paratyphi B (реакция Видаля) (рис. 3). В целом, при титрах антител 1:200 и выше подозревают брюшной тиф, особенно в случае положительной динамики уровня антител. Разработана система для выявления Vi-антител в реакции непрямой гемагглютинации. Полагают, что она позволяет выявлять носителей S. typhi не менее успешно, чем культура из фекалий.
Для специфической профилактики брюшного тифа в нашей стране используют убитую тифозную вакцину (готовят из штамма Ty2). Хорошие результаты дает применение Vi-антигена. Профилактическую иммунизацию проводят по эпидемиологическим показаниям, т.е. членам семей хронических бактерионосителей; населению, проживающему на территориях, где произошли вспышки брюшного тифа (уровень заболеваемости превышает 25 случаев на 100 тыс. населения); лицам, выезжающим в страны, эндемичные по брюшному тифу.
Этиотропная терапия показана только при системных (генерализованных) сальмонеллезных инфекциях, прежде всего при брюшном тифе. Применяют разные антибиотики — лучше всего фторхинолоны (ципрофлоксацин, офлоксацин и др.); дополнительно можно применять левомицетин, ампициллин, амоксициллин. Хорошо помогая в лечении заболеваний, антибиотики практически не влияют на носителей брюшнотифозных сальмонелл.
Иерсинии
Живу не мешаю, заденут — кусаю.
- Парадоксы и логика таксономики.
- Эпидемиология.
- Экологический дуализм энтеропатогенных иерсиний.
- Серовары и патовары.
- Экологически зависимая регуляция вирулентности.
Род Yersinia включает 11 видов, но только три из них (Y. pestis, Y. enterocolitica и Y. pseudotuberculosis) имеют отношение к патологии человека. Y. pestis (возбудитель чумы) занимает высшую ступень в табеле о рангах среди возбудителей особо опасных инфекций. Полагают, что за время известных пандемий чума унесла не менее 200 млн. жизней. Первая, юстинианова, пандемия началась в Египте в 542 г. н.э. и захватила Европу, Африку и Азию. Она продолжалась до 600 г. н.э. Вторая пандемия, известная как Черная Смерть, проникла в Европу из Азии в 1330—1346 гг. Она продолжалась почти 100 лет и оказала существенное влияние на культуру, политику и систему медицинского образования. Наконец, в 1855 г. в Китае случилась третья пандемия чумы, которая постепенно распространилась на Европу и Америку. В 1894 г. в Гонконге французский бактериолог А. Иерсен выделил возбудителя чумы, дав ему название Bacterium pestis. Это открыло путь для изучения экологии агента и его распространения среди людей. Была установлена абсолютная зависимость природной чумы от циркуляции в системе «блохи—млекопитающие», прежде всего «блохи—грызуны». Человек выступает в роли случайного хозяина. Заражение происходит через укусы блох или повреждения кожи. Спустя 2—6 дней поднимается высокая температура, возникает головная боль, озноб, появляются распухшие, болезненные лимфатические узлы (бубоны), расположение которых зависит от места проникновения инфекта. Процесс носит системный характер, часто наблюдается септицемия, угрожающая жизни. Без лечения болезнь может быстро закончиться смертью от септического шока. Сегодня в развитых странах встречаются единичные случаи бубонной (незаразной) чумы среди лиц, контактирующих с животными, особенно с дикими. Они поддаются лечению антибиотиками (прежде всего стрептомицином) и редко заканчиваются вторичной (септической) пневмонией, смертельной для больного и опасной для заражения окружающих, т.е. для начала эпидемии.
Y. pseudotuberculosis и Y. enterocolitica вызывают у человека пищевые инфекции — иерсиниозы. Их природным резервуаром тоже служат мелкие грызуны, от которых они выделяются с фекалиями, заражая окружающих животных и людей. Подобно возбудителю чумы, Y. pseudotuberculosis и Y. enterocolitica обладают лимфотропностью, но это проявляется после инвазии в пейеровы бляшки терминальной части подвздошной кишки и далее в абдоминальные лимфоузлы. Процесс выглядит как энтеропатогенность. В подслизистой оболочке формируются микроабсцессы, поднимается температура, возникают абдоминальные боли, рвота и диарея с кровяными жилками. Генерализация возможна только у иммунокомпрометированных больных.
Долгое время на основании ряда общих микробиологических (мелкие грамотрицательные палочки) и эколого-патогенетических (первичные патогены млекопитающих, прежде всего, грызунов) признаков возбудителей чумы и иерсиниозов относили к пастереллам. В 1954 г. состоялось «переселение» рода Yersinia в семейство Enterobacteriaceae. С внедрением в таксономику генетических маркеров эта позиция укрепилась и сегодня выглядит незыблемой, хотя некоторые из признаков (прежде всего экологическое своеобразие) ставят иерсинии в особое положение среди энтеробактерий. Психологически трудно уравнять микроб чумы с остальными (даже наиболее патогенными) энтеробактериями, и о нем обычно говорят отдельно, пренебрегая академической систематикой. Между тем, генетическая общность Y. pestis и Y. pseudotuberculosis (в меньшей степени — Y.enterocolitica) говорит об обратном. Есть мнение, что возбудитель чумы появился около 1500 лет тому назад на основе штамма Y. pseudotuberculosis, потеряв часть генов 70-килобайтовой плазмиды и усвоив две новых плазмиды — 96 и 110-килобайтовые. C тех пор он мало изменился, сохранив исходную клональность.
Иерсинии мельче других энтеробактерий. Это овоидные палочки, близкие к коккобациллам. Типичен полиморфизм, и в мазках из культуры обнаруживаются различные формы — от кокковидных до длинных нитей. Они окрашиваются биполярно, что также нехарактерно для классических энтеробактерий. Они подвижны (кроме Y. pestis) за счет перитрихиальных жгутиков, которые образуются при температуре ниже 30°С и исчезают при 37°С. Подобно всем энтеробактериям, иерсинии не образуют спор, а капсула (гликопротеин F1, закодированный в 110-килобайтовой плазмиде) имеется только у возбудителя чумы. Факультативные анаэробы, биохимически достаточно активны, сбраживая углеводы, многоатомные спирты и пр.). Это позволяет дифференцировать их на основе классических ферментативных тестов, принятых для разграничения родовых и видовых таксонов семейства Enterobacteriaceae. В отличие от других энтеробактерий иерсинии плохо растут на лактозных дифференциально-диагностических средах, давая мелкие лактозонегативные колонии-росинки.
Важный признак — двойственность экологии Y. pseudotuberculosis и Y. enterocolitica. Инфицируя широкий круг теплокровных животных (персистенция или патогенетически значимая инфекция), они способны и к автономному (сапрофитическому) образу жизни. Эта особенность, связанная с психрофильностью, во многом определяет эпидемиологию иерсиниозов. Фенотип (в том числе продукция факторов вирулентности) энтеропатогенных иерсиний во многом зависит от температурного режима, что принято использовать для их селективного накопления в инвитровых культурах.
Источником энтеропатогенных иерсиний для человека являются синантропные грызуны (мыши, крысы), свиньи, реже крупный и мелкий рогатый скот. Заражение редко (если вообще) возникает при прямых контактах с животными или больными людьми. Как правило, инфицирование происходит из сапрофитической фазы, после размножения бактерий в обсемененных пищевых продуктах. Это связано с нарушением санитарного режима в животноводческих хозяйствах, производственных комплексах, овощехранилищах, холодильниках, столовых и пр. Размножение иерсиний в условиях холодильника на корнеплодах (бактерии попадают сюда непосредственно из почвы) и других овощах создает опасность инфицирования через свежие овощные салаты (ряд вспышек псевдотуберкулезного иерсиниоза отмечено после употребления в пищу сырой капусты, полученной из овощехранилищ). В целом пребывание энтеропатогенных иерсиний в организме хозяина можно рассматривать как факультативный (случайный) паразитизм, не обязательный для реализации жизненной стратегии возбудителя.