Содержание
Ложную тревогу снимают при помощи иммуноблоттинга. В отличие от обычного ИФА, иммуноблоттинг не только выявляет антитела по принципу да-нет, но позволяет дифференцировать реакции с отдельными антигенами, которые предварительно рассортировывают на носителе (обычно нитроцеллюлозе) путем электрофореза. После обработки полоски носителя исследуемой сывороткой проводят обычный ИФА, т.е. проявляют связавшиеся с антигенами антитела при помощи меченых антииммуноглобулиновых антител.
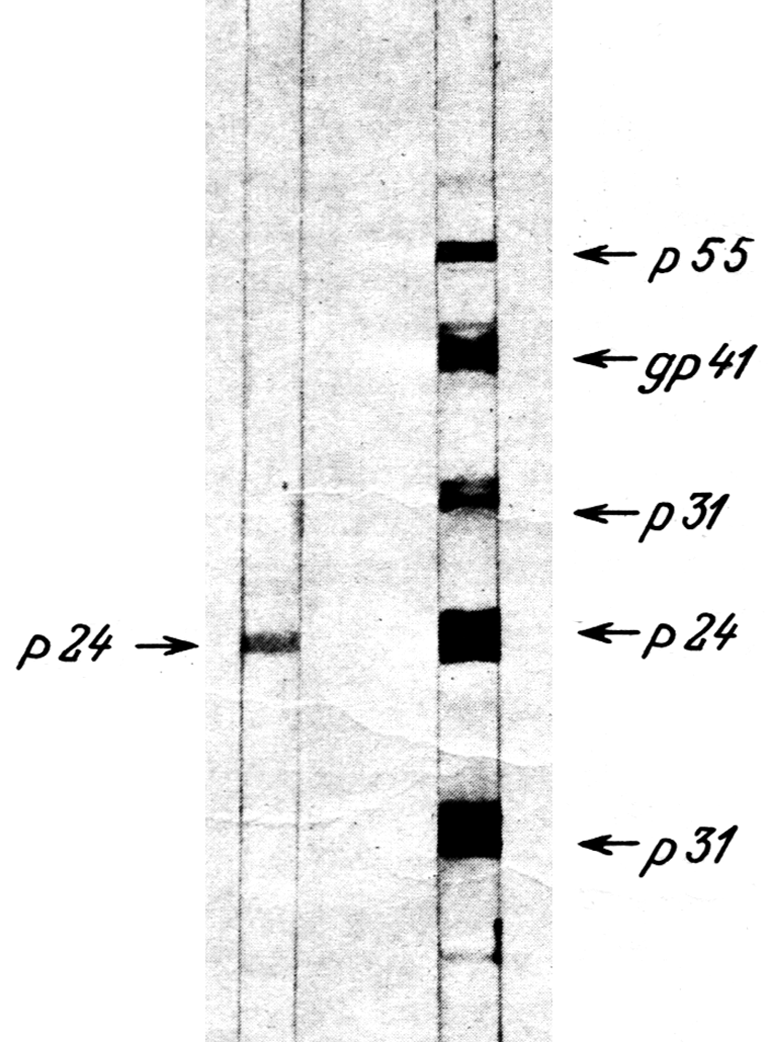
Положительные реакции выглядят в виде ИФА-пятен (англ. blot — пятно), каждое из которых соответствует дискретной паре антиген-антитело. Единственное пятно позволяет усомниться в истинности результата. Картину проясняет повторный анализ, сделанный через несколько месяцев. Усложнение спектра антител говорит о ВИЧ-инфекции, отсутствие динамики доказывает ложную позитивность первичного ИФА (рис. 7).
Дополнительно к иммуноблоттингу (или вместо него) для решения спорных вопросов пользуются прямыми ВИЧ-маркерами — присутствием в крови главного нуклеокапсидного белка (p24) и ВИЧ-генома (см. рис. 6). р24 определяют путем ИФА, ВИЧ-РНК — при помощи полимеразной цепной реакции.
Встречается и ложная серонегативность. Чаще всего это наблюдается в раннем периоде ВИЧ-инфекции в связи с отсроченной сероконверсией. Антитела обычно появляются в течение первых трех месяцев и могут отсутствовать, несмотря на вирусемию. Это так называемое диагностическое окно, продолжительность которого иногда затягивается на полгода и более (в редких случаях до года). Антитела нередко исчезают в терминальной фазе СПИДа, когда разрушение иммунной системы захватывает и ее гуморальное звено. В подобных случаях можно положиться на маркеры ВИЧ-репликации — р24 и РНК. Впрочем, к этому прибегают редко, так как можно либо подождать до появления антител, либо серопозитивность уже зафиксирована в анамнезе.
Антигенные и генетические различия между ВИЧ-1 и ВИЧ-2 требуют специальных для каждого из них тест-систем. Они могут быть объединены в общие диагностикумы, но суть от этого не меняется.
Принципы антивирусной терапии и проблемы вакцинации
Блокировать ВИЧ-репликацию научились вскоре после открытия вируса. Это удалось сделать при помощи аномальных нуклеозидов, подавляющих активность вирусспецифического фермента — обратной транскриптазы. Все ингибиторы подобного типа относятся к группе так называемых терминаторных субстратов, поскольку их эффект связан с обрывом (терминацией) синтеза ДНК на вирусной РНК-матрице. Наиболее известен азидотимидин (АЗТ; коммерческие названия — зидовудин, ретровир, тимазид), который до недавних пор был единственным средством, продлевающим жизнь больных СПИДом. Позже появились его клинические аналоги — ставудин, ламивудин, видекс, залцитабин и др.
Первый ажиотаж вокруг АЗТ быстро прошел. Виной этому оказалась высокая мутабельность вируса. На протяжении 6 мес в ВИЧ-популяции возникают разистентные клоны, которые захватывают лидерство в инфекционном процессе, сводя на нет эффективность терапии. Замена АЗТ на родственные препараты не достигает цели, так как все они блокируют один и тот же участок обратной транскриптазы, а потому попадают под общий механизм мутационной устойчивости.
В 1990 г. стали известны соединения ненуклеозидной природы, эффективно подавляющие обратную транскрипцию ВИЧ-1. Принципиально, что они взаимодействуют с участком молекулы, который, хотя и расположен по соседству с сайтом связывания для ингибиторов группы АЗТ, но мутирует независимо от него. Поэтому резистентность к АЗТ не распространяется на ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ). К сожалению, устойчивость к ННИОТ (например, к невирапину, ловириду, эфавирену и др.) формируется едва ли не быстрее, чем к нуклеозидным ингибиторам. Преимуществом является то, что привыкание в этом случае не носит универсального характера, т.е. резистентность к одному из ННИОТ не всегда распространяется на другие. В отличие от нуклеозидных ингибиторов ННИОТ действуют только на ВИЧ-1 и неэффективны против ВИЧ-2. Следуя логике, можно думать, что вирусу труднее выжить в среде с двумя разнотипными ингибиторами подобно тому, как развитие лекарственной резистентности у бактерий замедляется при сочетанном применении разных антибиотиков. Эта идея стимулировала разработку комплексной анти-ВИЧ-терапии, которая пришла на смену монотерапии нуклеозидными ингибиторами.
Дальнейшее развитие сочетанной анти-ВИЧ-терапии связано с торможением вирусспецифической протеазы. Как уже говорилось, этот фермент необходим для репликации вируса, превращая полипротеины в зрелые вирионные белки. Синтезировано множество соединений, блокирующих протеолитическую активность ВИЧ. Почти все они действуют по принципу пептидомиметиков, имитируя пептидную связь, атакуемую ВИЧ-протеазой. Протеазные ингибиторы (саквинавир, ритонавир, индинавир, нельфинавир, ампренавир, лопинавир и др.) вызывают быстрое и значительное снижение вирусной нагрузки. Недостаток прежний: продолжительность эффекта ограничена привыканием вируса. Уже через 6—12 мес после начала лечения в организме больных появляются устойчивые ВИЧ-варианты, причем резистентность, индуцированная одним препаратом, распространяется и на другие ингибиторы этого типа.
Таким образом, сегодня известны три группы клинически значимых ингибиторов ВИЧ-репликации. Они используют разные мишени и поэтому не вызывают перекрестной устойчивости вируса друг к другу. Кроме того, внутри одной из групп (ННИОТ) перекрестное привыкание возникает не во всех сочетаниях. Современные схемы (они получили название активного, даже агрессивного лечения) предусматривают тройную терапию на основе комбинации двух (нуклеозидного и ненуклеозидного) ингибиторов обратной транскриптазы и одного из антипротеазных препаратов. Применение такого коктейля ведет к быстрому падению вирусемии вплоть до уровня, не уловимого полимеразной цепной реакцией. Предлагаются и более громоздкие варианты — четырех и даже пяти препаратов. Усложнение идет за счет ННИОТ, не вызывающих перекрестного привыкания вируса.
Лечение рекомендуется начинать как можно раньше и продолжать возможно дольше. Для слежения за эффективностью терапии используют маркеры вирусной репликации, прежде всего количественные показатели РНК-вирусемии. Повышение титра ВИЧ-РНК говорит о необходимости возобновления или интенсификации лечения.
К сожалению, надежда на то, что многокомпонентная терапия обеспечит полную ВИЧ-стерилизацию организма, не оправдалась. ВИЧ сохраняет свой непредсказуемый мутационный потенциал тем более, что избирательность ВИЧ-ингибиторов не абсолютна, и при напряженной терапии сказывается их токсичность. Кроме того, интенсификация терапии делает ее дорогостоящей, о чем задумываются даже в экономически развитых странах.
И все-таки прогресс налицо. Он блистательно отражает связь между теорией и практикой, между тонкостями молекулярной биологии и клинической медициной. Кстати, задействованы еще не все вирусспецифические мишени, что вселяет надежду на очередные всплески ВИЧ-химиотерапии.