Содержание
В Российской Федерации ежегодно регистрируется от 5 до 20 случаев бешенства среди людей. За 1996 г. погибло 16 человек (Астраханская, Московская, Курская, Самарская области и др.). В 1997—1999 гг. в Москве зарегистрировано 3 случая смерти людей от бешенства.
Инфекция не зарегистрирована в Австралии, Новой Зеландии, на Гавайских островах, Ямайке, Кипре, Мальте, а также в Норвегии, Швеции, Финляндии, Испании и Португалии.
Вирион и репликация
Строение и внешний вид вириона возбудителя бешенства типичны для рабдовирусов (см. рисунок). Это частицы пулевидной формы, их размер 80—180 нм, имеют спиральный тип симметрии нуклеокапсида, относятся к оболочечным вирусам. Геном представлен одноцепочечной РНК (мол. масса 4,6·106 Да), которая упакована в комплексе с белком в виде спирали и окружена внешней оболочкой. На поверхности вирионов имеется множество мелких шипов. РНК, как у всех рабдовирусов, обладает негативной полярностью и имеет необходимую для синтеза мРНК РНК-зависимую РНК-полимеразу.
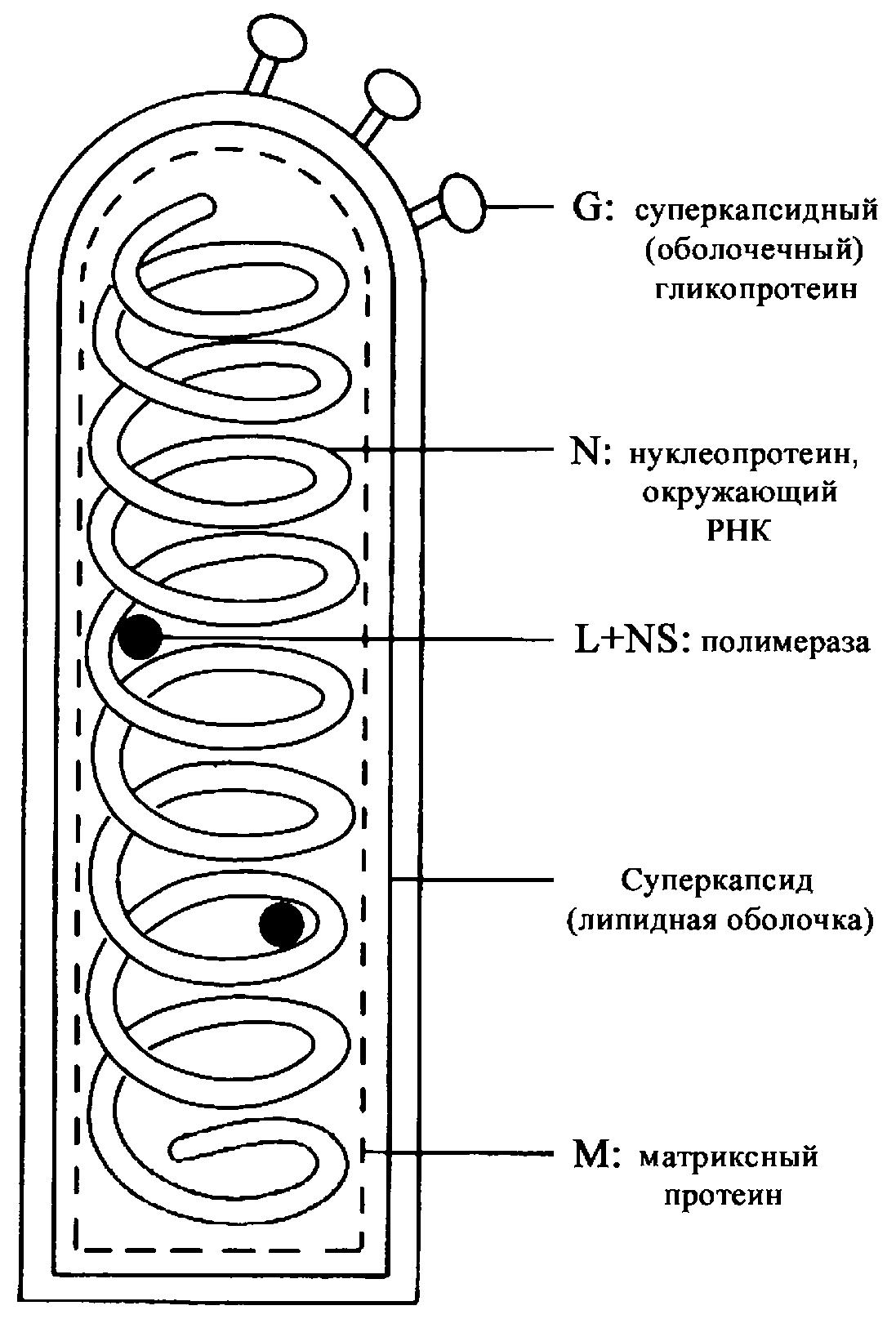
Вирион располагает пятью разновидностями белков, которые делятся на внутренние и поверхностные. К внутренним относятся белки N, M, L, NS. Белок нуклеокапсида (N, от англ. nucleocapsid) непосредственно связан с РНК и серологически идентичен у всех рабдовирусов. Одной из его функций является формирование рибонуклеопротеина, в составе которого РНК обретает устойчивость к клеточной РНК-азе. Он индуцирует образование комплементсвязывающих антител.
С нуклеокапсидом связано еще два белка сердцевины: L (от англ. large — большой) и NS (от англ. non structural — неструктурный), которые являются компонентами транскриптазы и в совокупности функционируют как полимераза. Белок L обеспечивает инициацию синтеза РНК, а NS-белок — их элонгацию.
Матриксный белок М (от англ. matrix) составляет внутренний слой липопротеиновой оболочки (суперкапсида) вириона, связывая его с сердцевиной. Его функцией является стягивание звеньев рибонуклеопротеина в цилиндр со спиральной симметрией. Белок М принимает участие в завершающей стадии морфогенеза вируса в зараженной клетке.
Поверхностный белок G (от англ. glycoprotein) представлен гликопротеином, входит в состав оболочки (суперкапсида) и структурно оформлен в виде колб диаметром 4,5—5,5 нм и длиной ножки 2 нм. Качественный состав белковой части молекулы варьирует в зависимости от вирулентности вируса. Например, в более вирулентном варианте аргинин замещается глутамином и изолейцином. Играет ведущую роль в процессах адсорбции на поверхности чувствительных клеток. G-белок является протективным антигеном, т.е. индуцирует образование вируснейтрализующих антител, которые блокируют адгезию вируса. Он также обладает гемагглютинирующими свойствами.
Вирион, прикрепляясь белком G к рецепторам чувствительной клетки, проникает в нее путем эндоцитоза, а не вследствие слияния суперкапсида с ее мембраной (у рабдовирусов нет белка, ответственного за этот процесс). Внутри клетки вирус обнаруживается в эндосомах, где при кислых значениях рН меняется конформация его G-белка, делая его чувствительным к клеточным протеазам. В результате ограниченного протеолиза обнажаются пептиды, вызывающие слияние суперкапсида вируса и эндосомальной мембраны. Благодаря этому нуклеокапсид освобождается и выходит в цитоплазму.
После раздевания начинается транскрипция. В эукариотических клетках нет РНК-зависимой РНК-полимеразы, поэтому для экспрессии своего генома рабдовирусы используют собственную полимеразу. Матрицей является РНК, прочно связанная с N-белком. Геном транскрибируется с образованием пяти моноцистронных мРНК. Это приводит к появлению мРНК, пригодных для трансляции, и в то же время позволяет регулировать количество отдельных мРНК. Каждый вирусный белок проходит свой путь созревания.
Репликация осуществляется в цитоплазме в две стадии. Минус-цепь в составе рибонуклеокапсида служит матрицей для синтеза комплементарной РНК, совпадающей по размеру с геномной. N-белок связывается с новосинтезированной РНК, образуя рибонуклеокапсид, содержащий плюс-геномную РНК. Затем процесс повторяется, и на плюс-РНК, как на матрице, образуются новые минус-цепи. В процесс репликации вовлечены N-, NS- и L-белки. Поскольку матрицы для транскрипции и для синтеза плюс-цепей в ходе репликации одинаковы, не удивительно, что эти процессы контролируются одними и теми же белками. Сердцевина вируса, состоящая из РНК, белков N, NS и L, собирается как отдельная структура в цитоплазме вместе с репликацией вирусной РНК и синтезом структурных (вирионных) белков.
Почкование зрелых вирионов — сложный процесс, для которого необходимы ассоциированный с мембраной G-белок, М-белок и рибонуклеопротеиновые частицы. Все они собираются на определенном участке мембраны. Ключевую роль в сборке и почковании играет М-белок. Он связывает рибонуклеопротеин и оболочку, кроме того, способен вызывать сворачивание удлиненных рибонуклеопротеиновых частиц с образованием той уплотненной конфигурации, которая присутствует в вирионах.
В системах in vitro и in vivo у вируса бешенства происходит формирование двух типов частиц: В (от англ. bullet — пуля) — зрелые полные вирионы и Т ( от англ. trunk — ствол) — дефектные интерферирующие частицы. Последние не обладают инфекционностью, имеют размер 60—80 нм и содержат приблизительно половину вирусного генома. Дефектные частицы размножаются только в присутствии полного вируса (В-частиц). Интерференция с В-частицами происходит на стадии репликации вирусной РНК.
Патогенез
Заражение происходит при укусе и/или ослюнении раны больным бешенством животным. Некоторое время (от нескольких часов до 6 дней) вирус находится в месте внедрения. Здесь он концентрируется в мионевральных синапсах и первичное размножение происходит в миоцитах или в эпителиальных клетках базального слоя эпидермиса. Далее вирус проникает в сенсорные и двигательные нервные окончания путем связывания с ацетилхолиновыми рецепторами нервно-мышечных синапсов. В этом месте нервные окончания не имеют миелиновой оболочки, что облегчает проникновение в них вируса. Путем пассивного центростремительного продвижения по аксоплазме нервных волокон он достигает центральной нервной системы, где внедряется в нейроны дорсальных ганглиев спинного, а затем и головного мозга, накапливаясь в нейронах гиппокампа, ядер моста, мозжечка, лимбической системы и обонятельных луковиц. Из ЦНС вирус диссеминирует по всему организму тем же путем, но уже в центробежном направлении. Уже за несколько дней до появления первых клинических признаков он может выделяться в окружающую среду через респираторный тракт, мочевыделительную систему, со слюной. В связи с богатой иннервацией слюнных желез титр вириона в секрете ротовой полости намного превышает его содержание в мозговой ткани. Выход в протоки слюнных желез обеспечивает передачу вируса со слюной при укусах. В крови вирус не обнаружен.
Входными воротами являются не только клетки поперечнополосатых мышц, нервно-мышечные бляшки, проприорецепторы сухожилий, но и рецепторы вкусовых сосочков языка и нейроэпителий обонятельных луковиц. Известны, в частности, случаи бешенства у спелеологов, занимающихся исследованием пещер. Здесь обитает большое количество насекомоядных летучих мышей — бессимптомных носителей вируса бешенства. Со слюной мышей он выделяется в окружающую среду и при вдыхании зараженного аэрозоля может вызвать заболевание.
Скрытая персистенция уличного вируса бешенства (для нее характерен слабый цитопатический эффект и непрерывный, но очень низкий уровень продукции вируса) выявляется также у собак, песцов, волков, грызунов, летучих мышей. Их укусы могут приводить к заболеванию и смертельному исходу. В процессе персистенции возможны изменения различных свойств вируса, в том числе повышение вирулентности, что способствует формированию новых эпидемически значимых вирусных штаммов.