Содержание
Аренавирусы имеют оболочечный вирион круглой или овальной формы, диаметром около 100 нм с колебаниями от 60 до 300 нм. Они содержат гранулярные частицы — клеточные рибосомы, давшие название вирусам (рис. 2).
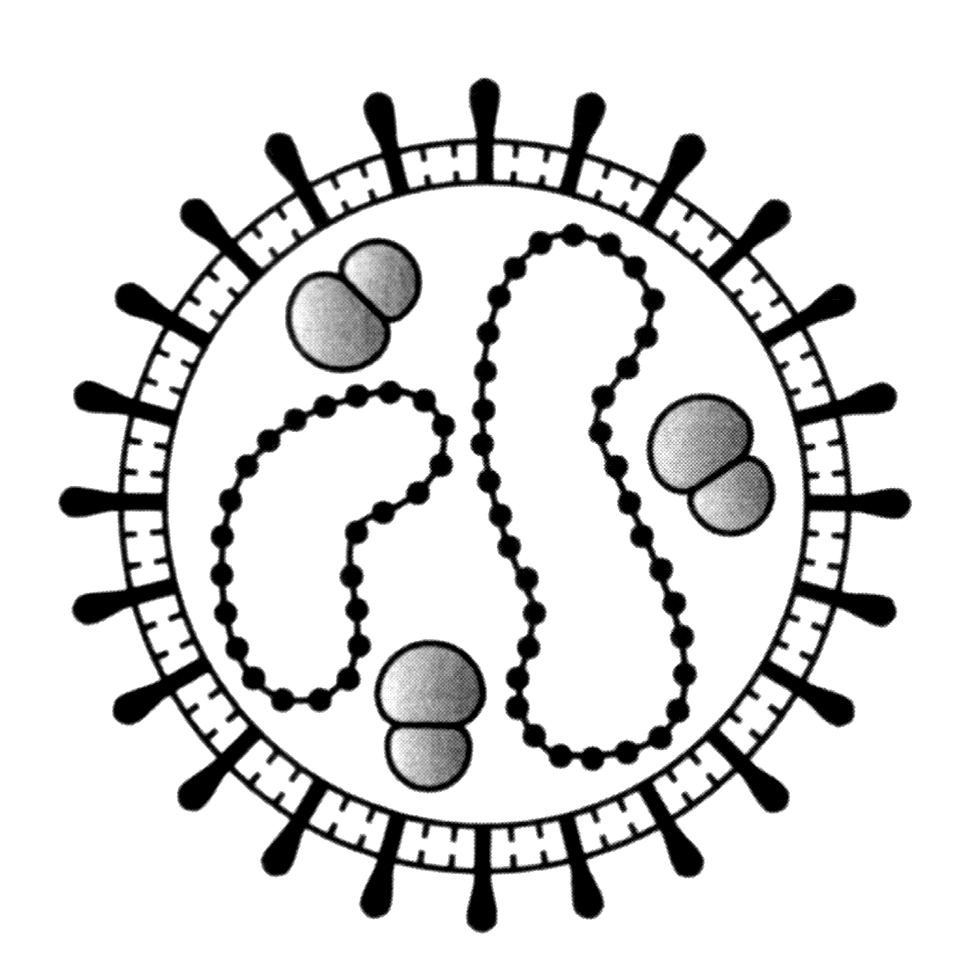
Роль рибосом не ясна, но они не определяют инфекционной силы вируса. Вирионная РНК состоит из двух циркулярных сегментов — L (англ. long) и S (англ. short) величиной 7,2 и 3,4 кбайт. Они находятся в спиралевидном комплексе с белком — N-протеином (англ. nucleocapsid). На поверхности вириона имеются шипы длиной около 10 нм, которые состоят из основания (гликопротеин G2) и головки (гликопротеин G1), связанной с G2 ионным взаимодействием. Белки N и G2 отличаются консерватизмом, определяя антигенные контакты между аренавирусами; для G1 характерна видовая и даже штаммовая специфичность. С вирусной частицей связаны также белки L (РНК-зависимая РНК-полимераза) и Z (функции неизвестны); их положение в вирионе не определено.
Репликация происходит в цитоплазме. РНК — односпиральна, отличается так называемой амбисенс-стратегией кодирования, т.е. ведет себя как минус- и плюс-РНК.
Поэтому хотя об аренавирусах принято говорить как о негативных РНК-вирусах, это неверно.
- Примерно половина S-сегмента ведет себя как минус-РНК, определяя синтез нуклеокапсидного (N) протеина.
- Другая часть является плюс-РНК, обеспечивая синтез предшественника поверхностных гликопротеинов.
L-сегмент вирионной РНК негативно кодирует L-белок, РНК-зависимую РНК-полимеразу, которая, в частности, определяет синтез небольшого (11 кДа) цинксвязывающего белка с неясными функциями.
Полипротеин после гликозилирования расщепляется на G1 и G2. Они встраиваются в плазматическую мембрану и служат местом взаимодействия с вирусным нуклеокапсидом. Обретая липидную оболочку (суперкапсид), вирус отпочковывается от клетки. G1 и G2 идут на построение вирусных шипов, предназначенных для взаимодействия с клеточными рецепторами, и служат мишенью для нейтрализующих антител.
Резервуаром для аренавирусов является хроническая инфекция грызунов. Заражение обычно проходит бесследно, причем лучшим вариантом является раннее инфицирование (плоды, новорожденные), когда организм отвечает иммунологической толерантностью на внедрение вируса. Возникает персистентная вирусемия, которая отражает недостаточный иммунный ответ у зараженных животных. Некоторые аренавирусы (например, вирус Ласса) используют механизм вертикальной передачи от матерей потомству. В других случаях раннее инфицирование достигается при сбрасывании в мочу вируса, что предполагает продолжение жизни аренавируса за счет заражения новых особей.
Человек является случайным хозяином аренавирусов. Заражение, как правило, не дает клинического результата, но иногда может иметь тяжелые, часто летальные последствия. О природноочаговом характере инфекций говорят названия основных аренавирусных болезней — Аргентинская (вирус Хунин), Боливийская (вирус Мачупо), Венесуэльская (вирус Гуанарито) латиноамериканские лихорадки, африканская лихорадка Ласса (вирус Ласса). Они отражают место первого описания болезней и их вирусов. Только лимфоцитарный хориоменингит избежал географической участи и распространен повсеместно через синантропных мышей.
По клинике большинство инфекций не выходит за рамки гриппоподобных заболеваний. После 10—14 дней инкубационного периода поднимается температура, возникают озноб, головная и мышечные боли, недомогание, боль в горле, артралгии. При тяжелых формах через неделю появляются симптомы геморрагического диатеза и поражений нервной системы (кожные и мукозальные петехии, кровотечения, рвота, диарея, дизурия, фотофобия, потеря слуха, иногда гепатит и др.). Повышение проницаемости капилляров ведет к оттоку плазмы в ткани, сгущению крови и шоку. Повреждение стволовых клеток костного мозга сопровождается лейкопенией и тромбоцитопенией (одна из причин геморрагического синдрома и кровотечений). В целом болезнь протекает благоприятно и заканчивается выздоровлением через 2—4 нед. Летальность — менее 2%.
Патогенез малопонятен. Гриппоподобные симптомы говорят о том, что аренавирусы, проникая через верхние дыхательные пути (контакт с высохшей мочой грызунов), вызывают повреждение респираторного эпителия. Размножение продолжается в регионарных лимфатических узлах, откуда вирусы попадают в кровь, где обнаруживаются в течение 3 нед после начала инфекции. Возбудитель присутствует в различных органах, но степень патологии не соответствует вирусологическим находкам. Попытки связать развитие болезни с иммунокомплексным воспалением оказались безрезультатными. Между тем, по аналогии с естественными хозяевами (грызунами) иммунологический конфликт должен играть важную роль в аренавирусной патологии. В опытах на мышах показано, что инфекция новорожденных ведет к длительной и безвредной персистенции вируса лимфоцитарного хориоменингита. Заражение взрослых особей вызывает острую смертельную нейроинфекцию, связанную с иммунными сдвигами, прежде всего в Т-клеточном звене иммунитета.
Учитывая контактную безвредность аренавирусов для клеток грызунов и человека, трудно допустить значение прямого цитопатического эффекта. Следует задуматься о медиаторах (тех же цитокинах), выделяемых зараженными клетками, и их участии в формировании дисфункций. В частности, мышей, зараженных летальной дозой вируса лимфоцитарного хориоменингита, удавалось спасти при обработке антителами к альфа/бета-интерферону. Это говорит о том, что эндогенные цитокины повышают патогенетическую активность аренавирусов, тем более что сами они мало чувствительны к действию интерферонов.
Элиминация аренавирусов у человека связана с нейтрализующими антителами, которые образуются чрезвычайно медленно, но, появившись, сохраняются долгие годы. Роль клеточного иммунитета в саногенезе при аренавирусных заболеваниях подлежит уточнению.
Клиническая диагностика аренавирусных инфекций (это относится ко всем арбо- и родентвирусным болезням) представляет большие трудности. Поэтому особое значение имеет специфическая диагностика, основанная на выявлении возбудителя и антивирусных антител. Материалом для выделения вируса служат кровь и спинномозговая жидкость больных, которые вводят в культуры клеток или интрацеребрально сосущим и только что отлученным от матери мышам и хомякам; при подозрении на лимфоцитарный хориоменингит и лихорадку Ласса используют взрослых мышей. О присутствии аренавирусов можно судить по наличию РНК в ПЦР с обратной транскрипцией. Для поиска вирусных антигенов применяют иммуноферментный тест. Наконец, возможно определение антивирусных антител. Из различных методов для этого лучше всего подходит реакция с энзиммечеными антителами.
Неспецифическая профилактика основана на борьбе с грызунами. Разработана живая аттенуированная вакцина из вируса Хунин, которая прошла успешное испытание на людях в странах, эндемичных по Аргентинской геморрагической лихорадке. Получена рекомбинантная вакцина для вируса Ласса. Она оказалась высоко протективной в опытах на зараженных обезьянах.
Вирус иммунодефицита человека
Его догнать пытался я, но он исчез,и снова появился, и вновь исчез…
- История открытия и происхождение.
- Вирион.
- Молекулярные и клеточные мишени.
- Взаимоотношения вируса с клеткой.
- Персистенция и агрессивность.
- Патогенез, патология, фазы инфекции.
- Синдром приобретенного иммунодефицита.
- Иммунитет: проигранная стратегия.
- Лабораторная диагностика.
- Принципы этиотропной терапии.
- Проблемы превентивной и стерилизующей вакцинации.
В 1981 г. Центром по контролю за заболева- емостью в США было сделано сообщение о том, что в течение восьми месяцев в Лос-Анжелесе зарегистрировано пять больных с редкой формой пневмонии, вызванной пневмоцистами — Pneumocystis cаrinii (сегодня их относят к грибам — см. «Медицинская микология»). Цифра впечатляла, так как за предыдущие десять лет было зарегистрировано всего два случая такой патологии. В связи с тем, что пневмоцисты не опасны для здоровых людей и проявляют агрессивность лишь на фоне ослабленного иммунитета, возникло подозрение о новом заболевании, которое спровоцировало иммунную недостаточность, осложненную пневмоцистозом. В отчете отмечалась еще одна подробность: все больные были молодыми гомосексуалистами.
Примерно тогда же были собраны данные о новых случаях саркомы Капоши. Ранее эту разновидность рака наблюдали у пожилых мужчин и лиц, принимавших иммунодепрессанты. На сей раз болели молодые гомосексуалисты. У некоторых из них саркома Капоши сочеталась с пневмоцистной пневмонией.