Содержание
Следует отметить, что эффективность всех оперативных вмешательств, несмотря на множество предложенных модификаций (около 50), оказалась недостаточно высокой в плане развития осложнений в послеоперационном периоде (рефлюкс-эзофагит, пептические язвы пищевода, стриктуры), а также рецидива заболевания. Все эти осложнения грубо нарушают качество жизни оперированных больных, приводя к потере трудоспособности, частой инвалидизации и требуют повторных сложных операций.
Неудовлетворенность результатами хирургического лечения ахалазии пищевода является основной причиной продолжающегося поиска новых способов оперативного лечения, в том числе и аллопластических видов кардиопластики. На смену утративших свою роль материалов (капроновых сеток, поливинил-алкогольной губки, консервированной твердой мозговой оболочки, брюшины и т.д.) приходят современные импланты — сплавы никелид-титана (Ручкин В.И., 2006), различные полипропиленовые сетчатые эндопротезы (Hobbman В., 1997; Галимов О.В., 2008) (рис. 10).
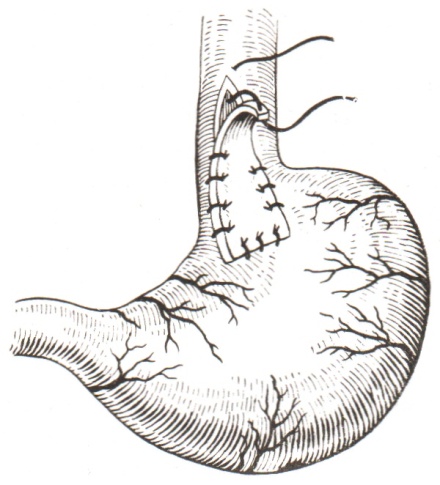
В последние годы за рубежом и в России получают широкое развитие видеоэндоскопические методики лечения различных болезней пищевода, в том числе ахалазии кардии, с использованием торакоскопии или лапароскопии. Эти доступы вызывают минимальную травму, о чем свидетельствуют менее глубокие нарушения показателей функции внешнего дыхания, системной гемодинамики и периферического кровообращения, кислотно-щелочного состояния и газового состава крови (Перескоков С.В., 2005).
Послеоперационный период в связи с этим протекает легко, быстрая выписка из больниц становится правилом, а возвращение к нормальной жизни происходит за 10–14 дней. Кроме того, из-за увеличения, даваемого видеоэндоскопической техникой, пищевод и окружающие структуры видны намного лучше, и точность выполнения этих операций возрастает.
Применение торакоскопии для лечения эзофагеальных болезней описал Hunter в 1985 г. М. Patti et al. (1995) представили первые опыты торакоскопической и лапароскопической миотомии пищевода и различных антирефлюксных методик при ахалазии кардии, выполнение которых также необходимо, как и при операциях открытым способом. Чаще применяется фундопликация по Дору (подшивание стенки дна желудка к краям миотомного разреза) как более легко осуществимая, а также используют типичную операцию Ниссена или гемифундопликацию по Toupet и др.
В России первую лапароскопическую операцию по методике Геллера-Суворовой произвел А.С. Балалыкин (1994). В настоящее время эндоскопическая хирургия при лечении ахалазии кардии применяется многими (Емельянов С.И., 2000; Марейко В.Д., Нечай В.С., 2002; Шипулин П.П., 2005; Алахвердян А.С., 2008 и т.д.).
Абсолютными противопоказаниями к выполнению эндохирургических вмешательств являются:
- Сердечно-легочная недостаточность в стадии декомпенсации (что является противопоказанием к наложению карбоксиперитонеума).
- Нарушения свертывающей системы крови, особенно в сторону гипокоагуляции.
- Цирроз печени.
Относительные противопоказания:
- Наличие кишечных свищей на передней брюшной стенке.
- Срединная лапаротомия в анамнезе.
Хорошие результаты после эндохирургических вмешательств отмечены в 80–95% случаев. Однако у 15–25% пациентов после таких операций наблюдается развитие рефлюкс-эзофагита (Robertson, 1995), а у 7–28% больных — рецидив дисфагии (Haussen M., 1990). Во время операции возможна перфорация пищевода, что в 3,6% случаев потребовало конверсии операции (переход на открытый способ — А.А. Никитин, 2005). Тем не менее большинство хирургов связывает дальнейший прогресс в лечении ахалазии кардии именно с эндоскопическими технологиями.
Особо трудным вопросом остается выбор лечебной тактики у пациентов с рецидивами заболевания как после пневматической дилатации, так и после хирургического вмешательства. Большинство авторов в этих случаях прибегают к повторным дилатациям на фоне полноценной медикаментозной терапии, при этом ни слабый желудочно-пищеводный рефлюкс, ни застойный эзофагит не являются противопоказаниями к данному способу лечения (Черноусов А.Ф., Царенко И.А., 1998).
Выполнение повторной операции при рецидивах целесообразно при отсутствии положительного эффекта от консервативного лечения и прогрессирования основного заболевания. Она преследует следующие цели: обеспечение проходимости желудочно-пищеводного перехода, восстановление замыкательной функции кардии путем реконструкции (по возможности) нормальных анатомических взаимоотношений.
Круг выполняемых реконструктивных операций весьма широк. Выбор методики определяется типом первого вмешательства, видом осложнения, принципиальным подходом хирурга к причинности осложнения, опытом и мастерством его и т.д.
Так, О.Д. Федорова еще в 1973 г. приводила сведения о 15 различных реконструктивных операциях, осуществлённых по поводу рецидива кардиоспазма. Предлагается выполнение достаточно сложных и травматичных операций: резекции кардии с перемещением пищевода в фундальный отдел желудка с созданием нового кардиального затвора (Вилявин Г.Д., 1971), резекции пищевода с пластикой его толстой кишкой (левой половиной), чаще с пластикой пищевода изоперистальтической желудочной трубкой (Черноусов А.Ф., 2005, 2008). К данным методикам нужно прибегать по самым строгим показаниям, так как летальность в этих случаях увеличивается.
Таким образом, совершенствование методик, разработка и внедрение новых способов хирургического лечения ахалазии кардии являются актуальной проблемой современной гастроэнтерологии.
Ведение послеоперационного периода у больных с ахалазией кардии
Функциональная травма и стресс приводят к выраженным сдвигам в системе гомеостаза, которые начинаются на операционном столе и продолжаются в послеоперационном периоде.
Катаболическая фаза метаболической реакции организма на травму продолжается 3–5 дней и сопровождается выраженными нарушениями всех видов обмена веществ, особенно водно-солевого, и кислотно-щелочного состояния. Начиная с 2–3-х суток после операции на первый план выступают изменения в белковом обмене, которые выражаются в распаде белков организма и уменьшении массы тела.
Коррекция нарушения всех видов обмена веществ проводится по общепринятым правилам ведения интенсивной терапии с учетом конкретных сдвигов, определяемых биохимическими анализами. Широко применяются различные схемы парентерального и раннего энтерального зондового питания.
Для профилактики и купирования болевого синдрома в первые 2–3 суток вводятся наркотические и ненаркотические анальгетики.
Одной из особенностей послеоперационного периода у больных ахалазией является то, что мышечный жом сфинктера привратника создает определенное сопротивление для продвижения желудочного содержимого. Для преодоления этого сопротивления необходимо наличие сохраненного тонуса пищевода и желудка, перистальтика же этих органов в первые дни послеоперационного периода угнетена вследствие операционной травмы.
Поэтому для постоянной эвакуации скапливающегося содержимого желудка, а также с целью декомпрессии обнаженного слоя пищеводно-желудочного перехода в желудок устанавливают назогастральный зонд, который удаляется при появлении клинических признаков восстановления моторно-эвакуаторной функции желудка (3–4-е сутки).
С этого момента больным разрешается прием жидкости через рот в объеме 500 мл в сутки. Количество жидкости постепенно увеличивается до 1,5 л к 5–6-м суткам. В эти же сроки назначается 2-й послеоперационный стол, с 7–8-го дня больных переводят на стол 1а по Певзнеру.
При слабой перистальтике кишечника назначают гипертонические клизмы, растворы убретида, прозерина или галантамина.
Проведение операций на верхнем этаже брюшной полости сопровождается нарушением функции легких (гиповентиляция, ателектаз, пневмония), что существенно ухудшает течение послеоперационного периода. С целью нормализации дыхания выполняют оксигенацию, массаж грудной клетки, дыхательную гимнастику, ингаляции средств, разжижающих мокроту.
Частота послеоперационных легочных осложнений, а также тромбоэмболических осложнений снижается на фоне ранней двигательной активности больных, в связи с чем активные движения (сидеть в постели, вставать) разрешают к концу первого дня, на второй день больные могут передвигаться по палате.
Кроме того, осуществляют мероприятия, направленные на профилактику тромбоэмболических осложнений: назначают антикоагулянты по схеме, практикуется бинтование нижних конечностей эластическим бинтом, используется компрессионное белье, аппарат для перемежающей компрессии вен нижних конечностей.
В случаях возникновения осложнений в послеоперационном периоде назначается соответствующее адекватное консервативное или хирургическое лечение.
После выписки из стационара больные должны находиться на диспансерном наблюдении с периодическим проведением полноценного инструментального обследования: рентгенологического, эндоскопического, эхографического и т.д. (в том числе комплекс общеклинических методов обследования). В случаях появления осложнений и развития рецидива требуется госпитализация больных в стационар, соответствующая терапия и выбор рациональной лечебной тактики. На протяжении всей дальнейшей жизни больной должен помнить о соблюдении рекомендаций, касающихся режима, диеты, трудоустройства и проведения общеукрепляющей терапии.
Заключение
Ахалазия кардии, несмотря на ряд новых сведений о заболевании, во многом остается патологией, не известной современной медицине:
- этиология и патогенез болезни полностью не установлены;
- механизмы, лежащие в основе функциональной непроходимости кардии, не выяснены (спазм, ахалазия?);
- открытым остается вопрос — не являются ли все функциональные заболевания пищевода (дискинезии, кардиоспазм, ахалазия кардии) проявлением одной патологии;
- отсутствуют методы диагностики болезни на доклинических стадиях, когда нейрогуморальные сдвиги минимальны, а лечение более эффективно;
- единая тактика, как и надежные способы лечения ахалазии кардии, отсутствуют. Неудачи отмечаются при всех видах лечения (медикаментозном, кардиодилатации, хирургическом), а главное — сохраняется летальность, хотя и минимальная.
Как видно, неясных вопросов при данном заболевании много, и можно лишь надеяться, что все они будут решены при дальнейшем развитии медицинской науки.